Глава 2
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1 Клинико-анамнестическая характеристика пациенток
Исследование выполнено в рамках реализации постановления Правительства Российской Федерации от 9 апреля 2010 г. № 220 и договора о выделении гранта Правительства Российской Федерации для государственной поддержки научных исследований, проводимых под руководством ведущих ученых в российских образовательных учреждениях высшего образования, научных учреждениях государственных академий наук и государственных научных центрах Российской Федерации № 14.W03.31.0009 от 13.02.2017.
Тип исследования – проспективное, когортное, обсервационное, аналитическое [216]. В ходе его проведения изучали возможные аутоиммунные и эндокринные реакции, а также связанные с ними изменения у эстетических и онкологических пациенток с операциями на молочной железе с использованием силиконовых имплантатов и без них.
В рамках работы были проанализированы исходы 119 эстетических хирургических коррекций формы и объема МЖ, а также лечебных и реконструктивных вмешательств на МЖ у 106 пациенток в сроки до, через 3, 6 и 12 месяцев после операций. Исследование было одобрено Этическим комитетом СПбГУ (выписка из протокола 02-126 от 30.06.2017, дополнения одобрены 20.06.2018 и 17.11.2019), а также локальными Этическими комитетами тех учреждений, где пациентки проходили обследование и лечение. Включение в исследование было добровольным, анонимным, с оформлением информированного согласия на участие в исследовании и на хранение биологического материала в Лаборатории мозаики аутоиммунитета СПбГУ, согласно дизайну исследования (рисунок 1).
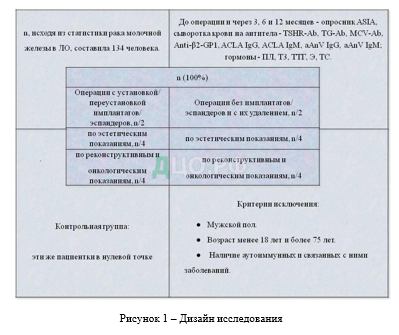
Все пациентки проходили предоперационное обследование и подготовку с применением рекомендованных стандартами оказания медицинской помощи клинических, лабораторных и инструментальных методов. Операции и последующее наблюдение за пациентками выполнялись на пяти клинических базах исследования, включая Центр пластической хирургии PARADA клиники
«Балтмед-Гавань», Санкт-Петербург; онкологическое отделение хирургических методов лечения № 2 Ленинградского областного онкологического диспансера (ЛООД), Санкт-Петербург; онкологическое отделение Клиники высоких медицинских технологий им. Н.И. Пирогова СПбГУ, Санкт-Петербург; Клинику пластической хирургии «БИОС», Москва; Клинику современной хирургии
«ЗДРАВА», Краснодар. Средний возраст женщин составил 39,2±11,4 лет. Пациентки включались в исследование и подвергались оперативному лечению
с сентября 2018 по ноябрь 2019 года с последующим наблюдением до года после операций. Показаниями к эстетическим операциям служили: постлактационная инволюция и/или птоз молочных желез, гипоплазия молочных желез, микромастия, асимметрия молочных желез, гигантомастия, тубулярная грудь, капсулярная контрактура, состояние после введения полиакриламидного геля с маститом (ПААГ-синдром), грудь сапожника, эстетическая неудовлетворенность формой и объемом молочных желез.
Онкологические и реконструктивные операции были выполнены пациенткам по следующим показаниям: фиброаденома, филлоидная аденома, организованная гематома молочной железы с подозрением на рак, спорадический рак молочной железы, генетически обусловленный билатеральный рак молочной железы (BRCA положительный), отсутствие молочной железы/молочных желез после лечения рака, семейный рак молочной железы, канцерофобия.
73 пациентки относились к группе молодого возраста от 18 до 44 лет. 15 пациенток – к группе среднего возраста от 45 до 59 лет. И 18 пациенток – пожилого и старческого возраста от 60 до 69 лет (таблица 2).
Таблица 2 – Характеристика пациенток по возрасту
| Параметр | Характеристика параметра | n (%) | ||
| Возраст по ВОЗ | молодой, до 44, n (%) | средний, 45-59, n (%) | пожилой, 60-74, n (%) | итого |
| Эстетика | 56 (52,8) | 1 (0,9) | 1 (0,9) | 58 (54,7) |
| Реконструкция | 12 (11,3) | 8 (7,6) | 11 (10,4) | 31 (29,3) |
| Онкология | 5 (4,7) | 6 (5,7) | 6 (5,7) | 17 (16) |
| Всего пациенток | 73 (68,9) | 15 (14,2) | 18 (17) | 106 (100) |
При этом 23 из 106 пациенток (21,7%) получали химиотерапию, 10 из 106
(9,4%) получали лучевую терапию, а 16 из 106 (15,1%) – гормонотерапию. Ввиду сведений о том, что пациентки эстетической маммопластики чаще, чем женщины соответствующих общих популяций подвержены привычке курения [146],
и принимая во внимание сведения о связи курения и аутоиммунитета [180], в частности – к щитовидной железе [229], при сборе анамнеза учитывался факт курения. Из 106 пациенток 35 были курящими (33%).
Среди пациенток, вовлеченных в исследование, были рапространены пирсинг и татуировки. Ввиду имеющихся данных об адъювантных эффектах материалов, применяемых при пирсинге и татуировках, а также о связи этих факторов с этиологией такого иммунопатологического заболевания, как саркоидоз, риск которого при наличии силиконовых имплантатов, по данным литературы, существенно повышен [56, 223, 236], мы отдельно учитывали, насколько часто встречаются эти факторы в анамнезе у сравниваемых пациенток. Оказалось, что 97 из 106 пациенток имели пирсинг (91,5%), а 38 (35,85%) – татуировки.
У пациенток с имплантатами количество единиц пирсинга было больше, чем у пациенток без них (2,5 против 2,2), но разница не была статистически значимой (р=0,073). Также не было статистически значимой разницы между ними и по количеству татуировок, равно как и по стажу их ношения. При этом никто из пациенток никогда не страдал саркоидозом.
25 пациенток имели кожные наполнители на основе гиалуроновой кислоты, еще 1 – на основе полиакриламидного геля.
Операции на молочных железах осуществлялись по описанным в ряде изданий общепринятым методикам [5, 18, 42, 112, 126, 178].
До операции (точка «0»), а также после нее – через 3 (точка «1»), 6 (точка «2») и 12 (точка «3») месяцев производили взятие периферической венозной крови из локтевой вены и анкетирование пациенток по опроснику ASIA (Приложение А). Сведения о пациентках и их лабораторных и инструментальных данных, получаемые при регулярном анкетировании и контрольных обследованиях, пополняли компьютерную базу данных со сроками наблюдения: до операции, через 3, 6 месяцев и 12 месяцев после нее.
За период наблюдения всего было выполнено 119 операций 106 пациенткам (таблица 3).
Таблица 3 – Распределение пациенток по наличию/отсутствию имплантата и по показаниям к операции
|
N п/п | Параметр | |||||
| операции с установкой/ переустановкой имплантатов/ эспандеров |
n (%) | операции без имплантатов/ эспандеров и с их удалением |
n (%) | итого по показаниям |
n (%) | |
| 1. | по эстетическим показаниям | 54 (45,4) | по эстетическим показаниям | 11 (9,2) | эстетическим | 65 (54,6) |
| 2. | по реконструктивным показаниям | 30 (25,1) | по реконструктивным показаниям | 3 (2,5) | реконструктивным | 33 (27,7) |
| 3. | по онкологическим показаниям | 6 (5) | по онкологическим показаниям | 15 (12,6) | онкологическим | 21 (17,7) |
| Итого | 90 (75,6) | 29 (24,4) | ||||
| Всего | 119 (100) | |||||
Всего было выполнено эстетических операций – 65, реконструктивных – 33, лечебных/онкологических без реконструктивного компонента – 21. Круглые имплантаты были использованы 74 раза, анатомические – 41, эспандеры – 24. Средний объем имплантата составил справа – 295 мл, слева – 320 мл. Положение имплантата было: частично под большую грудную мышцу (БГМ) и молочную железу (dual plane) – 44 случая, в 8 случаях – под фасцию большой грудной мышцы, в 31 случае – под БГМ и переднюю зубчатую мышцу, в 1 случае – под МЖ. Все пациентки получали периоперационную антибиотикопрофилактику цефалоспоринами 1-го поколения внутривенно за 30 минут до операции однократно, а при высоком риске инфекционных осложнений – до 72 часов [21, 22]. Дренаж устанавливался всем пациенткам со всеми видами операций, кроме операций по пересадке собственной жировой ткани (липофилинг),
где требовалось зашивание ран «наглухо». Срок стояния дренажа составил от 1 суток для операции по увеличению груди до 17 дней для мастэктомии.
В послеоперационном периоде на 119 операций встретились 7 осложнений (5,9%), потребовавших повторных операций. Еще 9 осложнений были купированы консервативной терапией (7,6%) (таблица 4).
Таблица 4 – Осложнения у исследуемых пациенток
| N п/п | Параметр | |||
| показания к операции | n (%) | осложнения, леченные оперативно, n (%) | осложнения, леченные консервативно, n (%) | |
| 1. | Эстетические | 65 (54,6) | 5 (4,2) | 3 (2,5) |
| 2. | Реконструктивные | 33 (27,7) | 2 (1,7) | 2 (1,7) |
| 3. | Онкологические | 21 (17,7) | – | 4 (3,4) |
| Итого | 119 (100) | 7 (5,9) | 9 (7,6) | |
| Всего | 119 (100) | 16 (13,5) | ||
А именно: несостоятельность швов/рубцов с последующей хирургической коррекцией произошла у 4 пациенток (3,4%). У 1 пациентки (0,8%) случилась несостоятельность вертикальных швов с обеих сторон. Еще у 1 пациентки (0,8%)
– с одной стороны. В обоих случаях это потребовало обработки раны с наложением вторичного шва. У 1 пациентки (0,8%), курильщицы, с имплантатами довольно большого объема разошлись края раны до снятия швов. Была выполнена санация периимплантатной полости с наложением вторичного шва. Еще у 1 пациентки (0,8%) произошло расхождение края раны в проекции зоны ЛТ (лучевой терапии) после замены эспандера на имплантат. Это потребовало укрепления мягких тканей грудной клетки сеткой и БГМ. У 1 пациентки (0,8%), заядлой курильщицы, после подтяжки молочных желез на имплантатах с коррекцией тубулярности, развился жировой некроз нижних квадрантов железы с частичным сквозным некрозом кожи. Это потребовало хирургической обработки раны, замены имплантата на эспандер с последующим его растяжением
физиологическим раствором. Далее была произведена замена эспандера на имплантат. В 1 случае в послеоперациеонном периоде развилась периимплантатная инфекция, закончившаяся удалением эспандера (0,8%). И, наконец, еще у 1 пациентки произошло смещение имплантата в сторону ключицы – его дистопия (0,8%). Это потребовало повторной операции – коррекции положения имплантата. В 9 случаях осложнения были купированы консервативно (7,6%): 3 серомы послеоперационного ложа (2,5%) – пункциями.
1 лимфоррея (0,8%) и 1 лимфоррея с гематомой (0,8%) после мастэктомий также были пунктированы. 2 случая галакторреи (1,7%) – терапией бромокрептином и перевязками. В 3-х случаях (2,5%) в послеоперационном периоде развилась периимплантатная инфекция, купированная антимикробной терапией. Важно отметить, что все случаи периимплантатной инфекции произошли в одном и том же отделении, в один и тот же период времени, и привели к изменению стандарта ведения таких пациенток в данном лечебном учреждении (таблица 5).
Таблица 5 – Осложнения у исследуемых пациенток и их коррекция
| N п/п | Осложнения | n (%) | Вид коррекции | n (%) |
|
1. |
Несостоятельность шва/рубца |
4 (3,4) | Обработка раны. Вторичные швы | 2 (1,7) |
| Санация периимплантатной полости, вторичные швы | 1 (0,8) | |||
| Укрепление мягких тканей грудной клетки сеткой и БГМ* | 1 (0,8) | |||
| 2. | Инфекция периимплантатной полости | 3 (2,5) | Антимикробная терапия | 2 (1,7) |
| Удаление эспандера | 1 (0,8) | |||
| 3. | Серома послеоперационного ложа | 3 (2,5) | Пункция серомы | 3 (2,5) |
| 4. | Галакторрея | 2 (1,7) | Перевязки, консервативная терапия | 2 (1,7) |
| 5. | Некроз нижних квадрантов железы | 1 (0,8) | Обработка раны. Замена имплантата на эспандер Замена эспандера на имплантат | 2 (1,7) |
Продолжение таблицы 5
| N п/п | Осложнения | n (%) | Вид коррекции | n (%) |
| 6. | Лимфоррея после мастэктомии | 1 (0,8) | Пункция лимфоцеле | 1 (0,8) |
| 7. | Лимфоррея с гематомой после мастэктомии | 1 (0,8) | Пункция лимфоцеле | 1 (0,8) |
| 8. | Дистопия имплантата | 1 (0,8) | Коррекция положения имплантата | 1 (0,8) |
| Всего | 16 (13,5) | Итого операций для коррекции | 8 (6,7) | |
| Примечание – * БГМ – большая грудная мышца. | ||||
Во всех случаях, кроме единственного (0,8%) – удаления эспандера, были достигнуты поставленные цели хирургического вмешательства.
Абсолютное и процентное отношение пациенток по наличию и отсутствию имплантатов на начало и конец исследования представлено в таблице 6.
Таблица 6 – Распределение пациенток по наличию/отсутствию имплантата в точках наблюдения (n=79)
| Импланты | До операции, n (%) | 12 месяцев, n (%) |
| Есть | 17 (21,5%) | 64 (81,0%) |
| Нет | 62 (78,5%) | 15 (19,0%) |
2.2 Характеристика методов исследования
2.2.1 Методы обследования пациенток
Все пациентки проходили общепринятое предоперационное обследование и подготовку с применением рекомендованных приказами Минздравсоцразвития
РФ клинических, лабораторных и инструментальных методов. Верификацию онкологического диагноза проводили на амбулаторном этапе. Алгоритм обследования больных включал клинико-лабораторные, рентгено- радиологические и ультразвуковые методы исследования. При сборе анамнеза в онкологической группе обязательно отмечали длительность заболевания, различие между паспортным и физиологическим возрастом пациенток, предшествующую противоопухолевую терапию, готовность пациенток к предстоящей реконструкции с учетом этапности операций, необходимости регулярных осмотров, введения физиологического раствора в эспандер для тканевой экспансии и необходимой замене на имплантат. Обсуждали возможные осложнения и борьбу с ними, а также альтернативные методы реконструкции молочной железы.
Лабораторная диагностика включала стандартную предоперационную подготовку: клинический и биохимический анализы крови, мочи, коагулограмму, определение группы крови и резус-фактора, реакции Вассермана, тесты на гепатиты В и С, ВИЧ.
Для выполнения задач исследования и оценки исходного иммуно- эндокринного статуса пациенток и возможных его изменений в динамике в сыворотке периферической венозной крови всех участниц исследования, до операции и во все контрольные сроки определяли содержание трийодтиронина (Т3), тиреотропина (ТТГ), эстрадиола (Э), тестостерона (ТС), пролактина (ПЛ), а также аутоантител к модифицированному цитруллинированному виментину (MCV-Ab), кардиолипину (ACLA IgG и ACLA IgM), бета2-гликопротеину 1 (Anti- β2-GР1), рецептору тиреотропного гормона (TSHR-Ab), тиреоглобулину (TG-Ab), аннексину V (aAnV IgG и aAnV IgM). Поскольку основным супрессором ТТГ и наиболее активным тиреоидным регулятором служит Т3 [32], содержание его предшественника тироксина (Т4) не учитывали. Измерения вышеназванных иммунных и гормональных параметров производили следующими методами: реакция непрямой иммунофлюоресценции, иммуноблоттинг, турбидиметрия, спектрофотометрия, иммуноферментный анализ в соответствии с рекомендациями
производителей наборов реактивов, предназначенных для этой цели («Алкор- Био», Россия – для гормональных; Euroimmun и Orgentec, Германия – для иммунных показателей). При выполнении исследования был использовано следующее лабораторное оборудование: полуавтоматический биохимический анализатор А15 (Biosystems, Испания), универсальный шейкер Elmi S-4, планшетный ИФА спектрофотометр BIOTECH, универсальный уошер ИФА планшетов Multiplate Thermo Scientific, оборудование для лайн-блоттингового анализа EuroBlot Master (Euroimmun, Германия), центрифуга-вортекс BS FV- 2400, комплекты автоматических пипеток на разные объемы производства компаний BioHit, Thermo Scientific, Sartorius, центрифуга Еppendorf c охлаждением 5415R, фармацевтический холодильник MPR-311 D Sanyo, дистиллятор «Циклон» WSC004, вытяжной шкаф Ruck Ventilatoren IP44/54, микроскоп люминесцентный EuroStar.
Инструментальная диагностика включала УЗИ молочных желез и регионарных лимфатических узлов или маммографию. Пациенткам с варикозной болезнью вен нижних конечностей выполнялось также УЗИ вен нижних конечностей. Всем пациенткам выполнялась флюорография/рентгенография органов грудной клетки. В группе пациенток с раком молочной железы дополнительно выполнялись маммография, УЗИ брюшной полости и КТ грудной клетки, что позволяло исключить отдаленные метастазы и/или контролировать лечение.
Морфологические методы применялись в случае первичной реконструкции и/или радикального лечения в группе онкологических пациенток для гистологической верификации опухоли. Это позволяло установить окончательный диагноз, уточнить стадию заболевания, распространенность опухолевого процесса, определить тактику лечения и объем оперативного вмешательства. Гистологическое заключение при РМЖ обязательно включало морфологический тип опухоли, степень дифференцировки опухоли, степень инвазии опухоли в окружающие ткани. Само морфологическое исследование операционного и биопсийного материала проводилось с использованием
гистологических и иммуногистохимических методик. После проводки по спиртам восходящей концентрации материал заливали в парафин и, после микротомирования, для гистологического исследования окрашивали с помощью гематоксилинэозина, а также пикрофуксина по Ван Гизону. Для иммуногистохимического исследования материал окрашивали с помощью толуидинового синего, а также проводили PAS-реакцию с контролем амилазой.
Кроме того, в соответвии с задачами исследования, а именно – изучить клинико-анамнестические характеристики пациенток до операции и в контрольных точках исследования, все его участницы оценивались по опроснику ASIA (Приложение А – опросник АСИА в переводе Леонида Павловича Чурилова) [19, 234]. В последующем выполнялась статистическая обработка данных опросника, что позволило судить о наличии или же отсутвии данного синдрома у пациенток до и в контрольных точках после операции [251].
Базами для лабораторной части работы послужили Лаборатория диагностики аутоиммунных болезней ПСПбГМУ им. акад. И.П. Павлова, а также Ресурсный центр развития молекулярных и клеточных технологий Научного парка СПбГУ.
2.2.2 Статистическая обработка данных
Для описания категориальных переменных использовались абсолютные значения и доли от целого – n (%). Остальные параметры описывались средним и стандартным отклонением (М(σ)), медианой, 1-3 квартилями (Md[q1;q3]), минимальным и максимальным значениями (min-max). Корреляционный анализ проводился при помощи коэффициента корреляции Спирмена (r-статистика). Сравнение данных с нормативными значениями проводилось одновыборочным критерием Манна – Уитни (W-статистика). Гипотеза равенства распределения частот проверялась точным критерием Фишера. Для оценки динамики
концентраций гормонов и аутоантител с учетом специфики больных использовалась бета-регрессия со смешанными эффектами (библиотека GLMMadaptive) [189]. Бета-регрессия была избрана как метод, предназначенный для моделирования данных, распределенных в интервале (0; 1) [85]. Для трансформации исходных данных использовалась унитизация с нулевым минимумом [232]. В качестве случайного эффекта использовались уникальные номера анонимизированных пациенток. Для оценки зависимости бинарных переменных или упорядоченных величин от независимых переменных использовалась логистическая регрессия с упорядоченным выбором [75]. Коэффициенты регрессий представлялись либо в нестандартизированном виде, либо в виде разницы контраста (b(se)).
Селекция моделей осуществлялась на основе информационных критериев Акаике (AIC) и Шварца (BIC). Модели характеризовались значениями логарифма максимального правдоподобия, девиансом и степенями свободы (Akaike’s ‘An Information Criterion’, AIC; log-likelihood, LR; degrees of freedom, df), причем оценивали значимость модели (p). Результат тестирования представлялся в виде коэффициента регрессии и его стандартной ошибки либо в виде их разницы в случае попарного сравнения (b(se)). Характеристика случайного эффекта и дополнительного параметра включала в себя соответствующее значение с 95%-м доверительным интервалом. В случае множественного тестирования гипотез использовалась поправка Беньямини – Хохберга для коррекции p-значений. Результаты считались статистически значимыми при p<0,05. Все расчеты производились на языке программирования R v3.6.1 [186].
