или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Содержание
- Список сокращений
- Введение
- 1. Характеристика ферментов поджелудочной железы
- 1.1. Поджелудочная железа крупного рогатого скота и ее ферментативная функция
- 1.2. Строение, свойства и механизм действия фермента трипсин
- 2. Выделение протеолитических ферментов из поджелудочной железы крупного рогатого скота
- 3. Технология производства препарата трипсин ООО «Самсон-Мед»
- 4. Методика определения качества готового препарата трипсин
- 5. Экологические и экономические аспекты производственного процесса
- 6. Техника безопасности и охрана труда
- Выводы
- Заключение
- Список литературы
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Список сокращений
КФ — классификация ферментов
ЛС — лекарственные средства
ПЕ — протеолитическая единица
ГФ — государственная фармакопея
ТП — технологический процесс
ВО — вспомогательные операции
ПО — переработка отходов
БАВ — биологически активные вещества
РНК-азы- рибонуклеаза
Кп — карбоксипептидаза А, Б
БАПНА- N-альфа-бензоил-DL-аргинин-4-нитроанилин гидрохлорид
ИЭТ – изоэлектрическая точка
Lys — лизин
Pro — пролин
Arg — аргинин
Glu – глутаминовая кислота
кДа — дальтон
Введение
При жизни животных некоторые органы способны накапливать биологически активные вещества. В мясной промышленности в процессе переработки животноводческого сырья получаются отходы, которые являются вторичным сырьем и используются при производстве ферментных препаратов.
Ферменты – это специфические катализаторы белковой природы, вырабатываемые клетками и тканями организмов. Они способны во много раз ускорять течение химических и биохимических реакций, не входя в состав конечных продуктов. Практические применения ферментов основаны на их высокой каталитической активности и более высокой по сравнению с небиологическими каталитическими системами субстратной специфичностью.
Производство ферментных препаратов, получаемых из органов животных, является одним из лидирующих направлений современной биотехнологии и относится к отраслям, объем продукции, которых постоянно растет, а сфера применения расширяется. Рост масштабов производства в данной отрасли ставит вопрос о переработки образующихся отходов мясокомбинатов, одним из которых является поджелудочная железа крупного рогатого скота. Поджелудочная железа крупного рогатого скота является ценным сырьем для производства ферментных препаратов, поскольку содержит протеолитические ферменты, среди которых наибольшее практическое значение имеют: рибонуклеаза, химотрипсин, трипсин, используемые в медицинской, фармацевтической и пищевой промышленности. Быстрое развитие связано с тем, что ферменты являются быстродействующими, нетоксичными биокатализаторами белкового происхождения, которые широко распространены в природе, без них невозможно осуществление многих биохимических процессов и жизнь в целом [10].
Протеолитический фермент трипсин, полученный из поджелудочной железы крупного рогатого скота, обладает выраженным противовоспалительным и противоотечным действием. Препарат трипсин эффективен при лечении гнойно-воспалительных процессов в хирургии различной локализации и этиологии, в офтальмологии расщепляет некротизированные ткани, способствует быстрому очищению раневых поверхностей. Кроме того, препарат трипсин повышает эффективность антибактериальной терапии за счет облегчения проникновения антибиотиков в ткани, обеспечивая их высокую концентрацию в очагах воспаления. Спектр применения трипсина может быть значительно расширен после тщательного изучения механизмов действия на функции различных органов и систем организма при патологических состояниях [11, 13].
Целью работы является: изучить технологические стадии производства протеолитического препарата Трипсин на основании технологического регламента на комплексное производство ферментных препаратов.
Задачи:
— изучить ферментный комплекс поджелудочной железы крупного рогатого скота.
— изучить строение и свойства фермента трипсин.
— освоить закономерности стадий извлечения поджелудочной железы из крупного рогатого скота, установить последовательности её обработки, консервирование.
— проанализировать протеолитическую активность Трипсина.
Объект и предмет исследований: Объектом исследований является поджелудочная железа крупного рогатого скота. Предметом является – фермент трипсин.
Глава 1. Характеристика ферментов поджелудочной железы
1.1. Поджелудочная железа крупного рогатого скота и ее ферментативная функция
Поджелудочная железа крупного рогатого скота (Pancreas) (рис 1.1.) – орган с двойной секрецией — внешней и внутренней. Внешнесекреторная часть поджелудочной железы вырабатывает панкреатический (поджелудочный) сок, принимающий участие в расщеплении белков, жиров и углеводов корма; внутрисекреторная часть железы продуцирует гормоны инсулин и глюкагон, регулирующие углеводный обмен, и гормон липокаин, принимающий участие в регуляции жирового обмена [21].
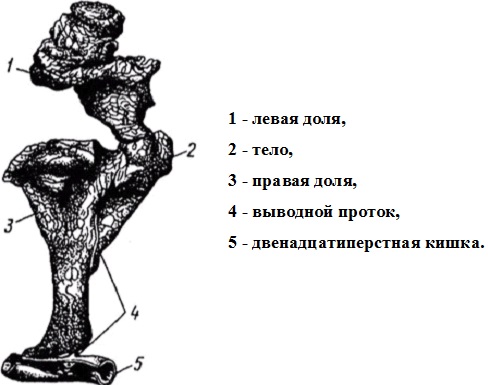
У крупного рогатого скота поджелудочная железа желто-бурого или розового цвета, в ней различают левую долю, тело и правую долю. Тело и правая доля поджелудочной железы лежат вдоль двенадцатиперстной кишки. Левая доля направлена перпендикулярно к ним и прилегает к рубцу. Выводной проток открывается в двенадцатиперстную кишку обособленно от желчного протока [22, 18].
Гистололическое строение. Поджелудочная железа — компактный орган, сложная застенная альвеолярная железа (рис.1.2). Сверху покрыта серозной оболочкой. Соединительнотканная строма образует тонкую капсулу, от которой отходят междольковые прослойки соединительной ткани. Внутридольковые прослойки из рыхлой соединительной ткани развиты слабо. В строме проходят сосуды и нервы, имеются мелкие вегетативные ганглии (скопления нервных клеток) и нервные окончания.
Экзокринная паренхима образована эпителием энтодермального происхождения и состоит из концевых отделов и выводных протоков. Концевые отделы имеют форму альвеол, образованы однослойным призматическим эпителием. Обычно в самый мелкий выводной проток, который называется вставочным протоком, открывается несколько альвеол. Такая структура называется ацинусом. Экзокринная часть железы, состоящая из ацинусов, носит название ацинозной паренхимы [4].
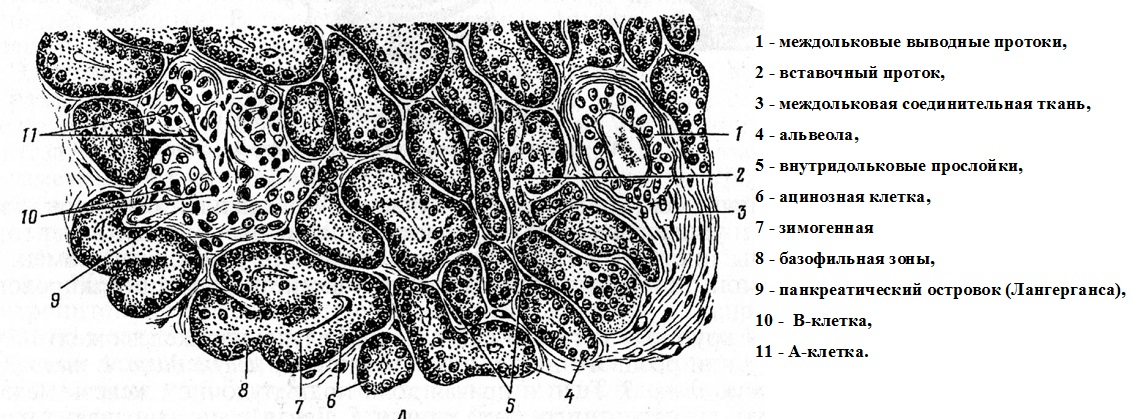
Ацинозная клетка имеет четко выраженную апикобазальную дифференцировку. Ее базальная, более расширенная часть заполнена массой плоских мешочков гранулярной цитоплазматической сети, воспринимает основные красители, за что называется базофильной, или гомогенной, зоной. Круглое ядро сдвинуто к базальной части клетки. Над ним расположен комплекс Гольджи. В апикальном полюсе клетки накапливаются крупные округлые гранулы секрета — зимоген, в который входят разнообразные ферменты в неактивной форме. Гранулы окрашиваются кислыми красителями, за что эта часть клетки названа оксифильной, или зимогенной, зоной. Секрет выделяется через апикальный полюс мерокринным способом и попадает в систему выводных протоков [4].
Выводной проток наименьшего диаметра назван вставочным, так как вдавливается на разную глубину в альвеолы. В результате клетки его стенки оказываются как бы вставленными в центр ацинуса и потому называются центроацинозными. На срезах их удлиненные светлые ядра можно видеть лежащими внутри альвеол. Диаметр вставочных протоков меньше альвеол. Их стенка образована уплощенными клетками со светлой цитоплазмой, бедной органеллами. Вставочные протоки объединяются сначала в мелкие внутридольковые выводные протоки, затем в более крупные внутридольковые протоки и, наконец, в междольковые выводные протоки. Последние образуют общий выводной проток поджелудочной железы, идущий к двенадцатиперстной кишке. По мере увеличения диаметра протока высота его эпителия увеличивается, а окружающие их прослойки соединительной ткани утолщаются и уплотняются.
Эндокринная паренхима составляет около 3% массы поджелудочной железы, представлена панкреатическими островками Лангерганса. Они имеют неправильно-округлую, эллипсоидную или отростчатую форму, хорошо снабжаются кровью. В островке обычно можно видеть несколько капилляров. Состоят островки из клеток нескольких типов, вырабатывающих разные гормоны. Друг от друга отличаются только при специальной обработке. Островковые клетки мельче ацинозных и светлее. Все они содержат мелкие митохондрии, хорошо развитый комплекс Гольджи и секреторные гранулы, характерные для каждого вида клеток.
Самые многочисленные В — клетки. Специальными красителями эти клетки окрашиваются базофильно. Их зернистость растворима в спирте и нерастворима в воде. Вырабатываемый ими инсулин способствует утилизации глюкозы тканями и превращению ее в гликоген, чем снижает уровень глюкозы в крови. А-клетки при специальной обработке окрашиваются оксифильно, растворимы в воде и нерастворимы в спирте. Эти клетки вырабатывают глюкагон — гормон, противоположный по действию инсулину. Он способствует расщеплению гликогена до глюкозы и выведению ее в кровь. Среди остальных клеток различают еще несколько типов, вырабатывающих гормоны, по-видимому, регулирующие белковый и липидный обмены [4].
Секрет поджелудочной железы содержит сложный набор гидролитических ферментов действующих на различные классы веществ – белки, жиры, нуклеиновые кислоты, углеводы. Некоторые ферменты (нуклеазы и амилазы) секретируются в поджелудочный сок сразу в активном состоянии, а другие ферменты — протеазы, фосфолипаза синтезируются тканью железы в виде неактивных предшественников–зимогенов и превращаются в активные ферменты уже в самом поджелудочном соке [14]. Известно, что поджелудочная железа крупного рогатого скота содержит целый ряд ферментов различной субстратной спецификации, в частности трипсин КФ (3.4.21.4), химотрипсин (3.1.1.3), карбоксиполипептидазы (КФ 3.4.16.1), рибонуклеазы.
Трипсин расщепляет белки до аминокислот и выделяется в виде неактивного трипсиногена, который активируется ферментом кишечного сока энтерокиназой. Химотрипсин расщепляет белки и полипептиды до аминокислот и выделяется в форме неактивного химотрипсиногена; активируется трипсином. Карбоксипептидаза действует на полипептиды, отщепляя от них аминокислоты. Рибонуклеаза – деполимеризует РНК до кислотно-растворимых моно — и олигопептидов.
Химотрипсин — протеолитический фермент, секретируемый поджелудочной железой в тонкий кишечник в виде неактивного предшественника – химотрипсиногена. Химотрипсин был исследован более детально, чем другие очищенные ферменты. Относительная молекулярная масса химотрипсина составляет 23000 Да, рН-оптимум 7,0-9,0, температурный оптимум около 50°С, ИЭТ молекулы химотрипсина составляет рН 8,1-8,2. Подобно трипсину химотрипсин осуществляет гидролиз субстратов сложных эфиров, который идет через образование ковалентного промежуточного соединения. Наряду с пептидами фермент гидролизует амиды и эфиры, при этом он предпочтительно расщепляет связи, образованные остатками ароматических аминокислот: тирозином, триптофаном, фенилаланином [23].
Карбоксипептидазы (А, Б) – протеолитеческие ферменты, экзопептидазы.
Карбоксипептидазы А и Б синтезируются в поджелудочной железе в виде проферментов прокарбоксипептидазы А и прокарбоксипептидазы В, в таком виде, в составе панкреатического сока ферменты попадают в двенадцатиперстную кишку, где под воздействием трипсина прокарбоксипептидазы А и Б превращаются в Карбоксипептидаза А и Б.
Карбоксипептаза А (КФ 3.4.17.1) состоит из 307 аминокислотных остатков, имеет молекулярную массу около 34 400 Да и отщепляет от пептидов все С-аминокислотные остатки, за исключением аргинина, лизина, пролина и гидроксипролина, катализируя, в основном, ароматические и алифатические аминокислоты. Карбоксипептидаза Б (КФ 3.4.17.2) состоит из 300 аминокислотных остатков, имеет молекулярную массу около 34000 Да и отщепляет только С-концевые остатки аргинина и лизина, катализируя основные аминокислоты [23].
РНК- аза – фермент — нуклеаза, выделяемый из поджелудочной железы крупного рогатого скота, катализирующие деградацию РНК. Это белок с молекулярной массой 14 кДа, состоит из 124 аминокислотных остатков, соединенных в одну полипептидную цепь, оптимум рН 7,4-7,5, ИЭТ — 9,6. Наличие четырех дисульфидных связей скрепляет макромолекулу фермента и придает ей устойчивость. Установлена трехмерная структура рибонуклеазы и осуществлен ее химический синтез. Процесс разрушения РНК панкреатической рибонуклеазой протекает в несколько стадий. Вначале фермент расщепляет межнуклеотидные связи неспирализованных участков полинуклеотидной цепи с образованием олигонуклеотидов. При этом гидролизуются связи между фосфором и углеродом (С) рибозного остатка с последующим трансфосфорилированием внутри молекулы и образованием циклических фосфорных производных. Далее рибонуклеаза гидролизует циклические фосфодиэфирные связи с образованием фосфатных производных. Эта реакция протекает медленно. Панкреатическая рибонуклеаза гидролизует межнуклеотидные связи избирательно в зависимости от природы азотистых оснований, входящих в нуклеотиды. Фермент предпочтительнее расщепляет фосфоэфирные связи пиримидиновых нуклеотидов в молекуле РНК. Рибонуклеаза с большой скоростью гидролизует фосфодиэфирные связи в нуклеотидах, содержащих в качестве азотистого основания цитозин [24].
1.2. Строение, свойства и механизм действия фермента трипсин
Трипсин (trypsinum) – ферментный препарат протеолитического действия, получаемый из поджелудочной железы крупного рогатого скота. Впервые кристаллический бычий трипсин (КФ 3.4.4.4) был получен Дж Х. Нортропом и М. Кунитцем в 1931 году [14]. При медленном нагревании до 25°С холодного насыщенного раствора белка в сульфате аммония выделялись квадратные пластинки кристаллов трипсина (рис 1.3.) [14].
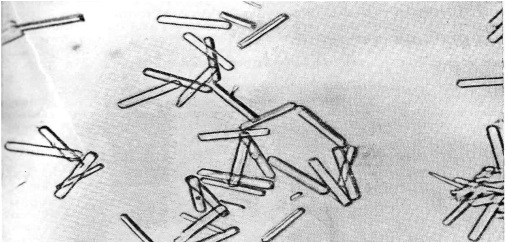
Строение и свойства трипсина. Трипсин содержится в поджелудочной железе в виде предшественника фермента — зимогена, называемого трипсиногеном. Молекулярная масса трипсиногена 23,023,8 кДа. Под действием энтерокиназы (К.Ф. 3.4.21.9) (протеолитическпй фермент, входящий в кишечный секрет) в кислой среде трипсиноген превращается в трипсин за счёт отщепления полипептида с шестью аминокислотными остатками с N-концевой части пептидной цепи. Трипсиноген может активироваться и трипсином. Процесс превращения трипсиногена в трипсин стимулируется ионами Са2+ при рН среды менее 4,0. Процесс этот в определенных условиях может стать автокаталитическим. Чтобы иметь возможность из активированного трипсиногена получить кристаллический трипсин, важно не допустить образования неактивного белка и активных фрагментов трипсина, которые имеют меньшую удельную активность, чем истинный трипсин. Для обеспечения нормального течения процесса превращения трипсиногена в трипсин необходимо предотвратить автолитические процессы в сырье в период хранения, обеспечить отсутствие химотрипсина, и соблюдать условия кристаллизации трипсина [5].
Трипсины от разных видов животных имеют близкий качественный и количественный набор аминокислот и форму кристаллов. Молекулы трипсина и трипсиногена имеют глобулярное строение. Бычий трипсин представляет собой белки с сильно выраженными основными свойствами, ИЭТ около pH 10,5, оптимум каталитической активности наблюдается в интервале рН 7,0-9,0, при температуре около 50°С. Относительная молекулярная масса бычьего трипсина 23,8 кДа и состоит из 223 аминокислотных остатков, образующих одну полипептидную цепь, содержащую шесть дисульфидных связей. Последовательность аминокислотных остатков фермента полностью расшифрована [3]. С помощью рентгеноструктурного анализа установлена третичная структура трипсина. Он относится к группе сериновых протеиназ и содержит в активном центре остатки серина и гистидина. Важным свойством молекул трипсина в растворе является их способность к ассоциации, в которой активный центр не участвует [16].
На ферментативную активность фермента трипсин и конформацию фермента и его зимогена влияют различные внешние факторы. Активность трипсина подавляется фосфорорганическими соединениями, некоторыми металлами, а также рядом высокомолекулярных белковых веществ — ингибиторов трипсина, содержащихся в тканях животных. Ионы Ca2+, Mg2+, Ва2+, Sr2+, Мn2+ повышают гидролитическую активность трипсина [8].
Трипсин способен превращать в активные ферменты все проферменты поджелудочной железы (трипсиноген, химотрипсиноген, прокарбоксипептидазу), а также фосфолипазу, и в связи с этим занимает ключевое положение в системе пищеварительных ферментов [16].
Биосинтез фермента трипсин. Трипсиноген это неактивное состояние трипсина. При попадании трипсиногена в двенадцатиперстную кишку, под действием желчи и фермента энтеропептидазы, который вырабатывают клетки слизистой оболочки кишечника (энтероциты). Фермент энтеропептидаза отщепляет с N — конца полипептидной цепи шесть аминокислотных остатков (Вал — (Асп)- Лиз. В процессе отщепления гексапептида от предшественника — важное биологическое значение, так как при этом происходит формирование активного центра и образование трехмерной структуры трипсина (схема 1.4.).
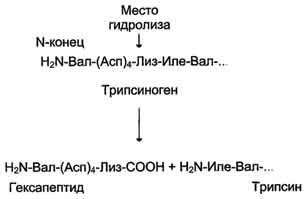
Механизм действия трипсина. Трипсин катализирует гидролиз преимущественно пептидных связей в молекулах белков, где карбоксильная группа образована аминокислотами с положительно заряженной боковой цепью – аргинином и лизином. При физиологических значениях рН трипсин подвергается автолизу с потерей ферментативной активности [3]. Пептидные связи Lys-Pro и Arg-Pro устойчивы к гидролизу. Частичной устойчивостью к гидролизу трипсином обладают некоторые другие пептидные связи, например, в структуре Lys-Lys-X связь Lys-Lys или связи в пептидах Arg-Arg, Arg-Lys и Lys-Arg. «Скопление» основных аминокислот в определенных участках пептида обусловливает частичную устойчивость его к гидролизу. То же самое справедливо и для пептидных связей Lys-Glu и Arg-Glu [9]. Специфичность триптического гидролиза позволяет «управлять», биохимической реакцией внося те или иные изменения в структуру гидролизуемых соединений. Например, по мере аминоэтилирования свободных SH-групп увеличивается число NH-групп и, следовательно, увеличивается количество пептидных связей, чувствительных к трипсину, то есть в гидролизате оказывается больше триптических пептидов.
Новейшим методом обратимого блокирования -NH2-групп считают реакции малеинирования и цитраконилирования. При необратимом заблокировании NH-группы лизина, трипсин может гидролизовать только те пептидные связи, в которых участвует аргинин. В этом случае в гидролизате обнаруживаются крупные аргиниловые пептиды. При обратимом блокировании остатков лизина, например, путем трифторацетилирования, после выделения аргиниловых пептидов их можно деблокировать, а затем подвергнуть триптическому гидролизу; при этом будут расщепляться только пептидные связи лизина [9].
Амиды расщепляются трипсином быстрее, чем пептиды, а сложные эфиры — быстрее, чем амиды. На скорость гидролиза эфиров не влияет природа спиртовой группы. Даже такое простое соединение, как этиловый эфир лизина, быстро гидролизуется трипсином. Замещение аминогруппы в боковой цепи делает гидролиз невозможным, тогда как замещение -аминогруппы, наоборот, благоприятствует гидролизу. В то же время, при удалении -аминогруппы гидролиз оказывается невозможным.
Специфические требования трипсина могут быть удовлетворены даже если необходимые группы находятся на разных молекулах. B. Инагами и Дж. Мураки [9] исследовали влияние некоторых четвертичных катионов на катализируемый трипсином гидролиз пептидов. Все исследованные катионы оказались конкурентными ингибиторами гидролиза специфических субстратов, например, этилового эфира бензоил-L-аргинина. Однако гидролиз ацетилглицина ускорялся в 3,9 по 2 раза метиламином, этиламином и 1-н-пропиламином соответственно, но 1-н-бутиламин оказался ингибитором. При взаимодействии с соответствующим ионом происходит активация трипсина, при этом сродство к субстрату не изменяется. Положительно заряженная группа индуцирует активацию каталитического участка фермента подобно тому, как это осуществляют боковые группы аргинина или лизина у специфических субстратов.
2. Выделение протеолитических ферментов из поджелудочной железы крупного рогатого скота
Сырьем для производства ферментных препаратов служит ферментное сырье – поджелудочная железа (орган двойной секреции) крупного рогатого скота. Поджелудочную железу собирают только от здоровых животных после ветеринарного освидетельствования их перед убоем и ветеринарной экспертизы.
Важнейшее условие правильной организации сбора ферментного сырья — быстрое извлечение его из туши животного. Время с момента извлечения поджелудочной железы до замораживания не должно превышать 1,5 часа, иначе активность сырья резко снижается. Первичная обработка сырья предусматривает очистку (препарирование) от посторонних тканей, прирезей и оболочек. Перед этим поджелудочную железу сортируют, устраняют имеющиеся дефекты. Препарируют сырье раздельно по видам скота и видам желез в специальном помещении эндокринного отделения мясокомбината. Помещение должно иметь хорошее освещение, температуру воздуха не более 18°С. Не допускается попадание на обрабатываемое сырье прямых солнечных лучей. Стены должны быть покрыты масляной краской, пластиком или облицовочной плиткой [17].
Поджелудочную железу крупного рогатого скота сначала отделяют от селезенки, двенадцатиперстной кишки, брыжейки и печени вручную или с помощью ножниц, острого ножа. Делают это осторожно, чтобы не повредить паренхиму. После этого железу раскладывают на столе и от нее отделяют остатки соединительной ткани и жира, сосудов, лимфатических узлов [7].
Технология хранения ферментного сырья. Для сохранения целевых биологических свойств ферментного сырья его немедленно после сбора и очистки консервируют. Применяемые способы консервирования должны быть такими, чтобы свести к минимуму структурные и физико-химические изменения свойств сырья, полностью предотвратить развитие микробиологических процессов и в максимальной степени затормозить биохимические процессы в тканях. Замораживание является наиболее распространенным методом консервирования, так как позволяет сохранить биологическую активность сырья. Для этого сырье замораживают в скороморозильных аппаратах и направляют в специальные морозильные камеры или в изотермический контейнер для транспортирования. В некоторых случаях применяют химическое консервирование этиловым спиртом, чистым ацетоном, формалином и поваренной солью. Замораживание ферментного сырья проводят от 40 до -50°С; иногда допускается замораживать при -20°С. Подготовленное и рассортированное сырье, предназначенное для замораживания, раскладывают в один или два слоя на противни из нержавеющей стали или алюминия. Длительность замораживания зависит от условий замораживания и величины желез. Ферментное сырье можно замораживать в морозильных аппаратах или в камерах, предназначенных для замораживания субпродуктов, при температуре не выше -20°С [7].
Активность эндокринно-ферментного сырья сохраняется при использовании аппаратов с иммерсионным или струйным распылением жидкого азота. Замороженное эндокринно-ферментное сырье упаковывают непосредственно в морозильной камере в деревянные ящики в количестве не более 30 кг или короба из гофрированного картона в количестве не более 10 кг. Ящики предварительно охлаждают и выстилают полиэтиленовой пленкой или пергаментом. Сырье в ящики укладывают плотно, не допуская излишних деформаций. Тару снаружи маркируют. Замороженное эндокринно-ферментное сырье хранят в камерах при температуре не выше -20°С в течение 4-6 месяцев. Перед отправкой на предприятия фармацевтической промышленности эндокринные железы подлежат ветеринарно-санитарной экспертизе. При наличии признаков гнилостного разложения или постороннего запаха, эндокринное сырье направляют для технической утилизации [7].
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
