Введение
Актуальность работы. В связи с ростом количества забракованных и фальсифицированных лекарственных средств особое значение придается обеспечению качества лекарственных средств на всех этапах их обращения.
В наше время для жителей мира охрана здоровья имеет большое значение, соответственно один из важных секторов для охраны здоровья является наличие лекарственных препаратов.
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
В законодательные акты были внесены изменения, которые определяют порядок ввоза на территорию ЕАЭС лекарственных средств. Евразийская экономическая комиссия (ЕАК) приняла решение об упрощении процедуры ввоза лекарственных средств. Выпуск препаратов и субстанций для внутреннего потребления, переработка для внутреннего потребления, реимпорт и другие процедуры будут осуществляться при условии, что лекарственные препараты и фармацевтические субстанции включены в Государственный реестр лекарственных средств государства – члена ЕАЭС.
Ранее при ввозе лекарственных средств на территорию России необходимо было получить разрешение Росздравнадзора и лицензию Минпромторга России. В настоящее время, в соответствие с новым нормативным актом, для ввоза партии лекарственных препаратов будет достаточно сведений о них, содержащихся в Государственном реестре лекарственных средств.
При этом получение сведений из реестра будет организовано на основе системы межведомственного электронного взаимодействия (СМЭВ) между Федеральной таможенной службой и Министерством здравоохранения и Министерством труда и социальной защиты РФ.
Это нововведение упростит документооборот компаний и при этом не повлечет увеличения потока «серого» импорта на отечественный рынок, а также других значительных перемен.
Решение о внесении изменений в положение о порядке ввоза на таможенную территорию ЕАЭС лекарственных средств и фармацевтических субстанций было принято на заседании Евразийской экономической комиссии. Положение касается юридических лиц и физических лиц – предпринимателей, иностранных организаций – производителей лекарств и физических лиц, осуществляющих ввоз таких товаров для личного пользования. Мера не распространяется на наркотические средства, психотропные вещества.
В связи с отменой лицензии ведомства на ввоз лекарственных средств цены на них не изменятся. Участники рынка одобряют некоторое упрощение правил ввоза лекарственных средств, предназначенных для проведения клинических исследований, проведения экспертизы лекарственных средств, для осуществления государственной регистрации препаратов. Вместе с тем новые правила импорта лекарственных средств, по мнению экспертов, не свободны от недостатков действующих норм. Перечень лекарственных средств и фармацевтических субстанций, ввоз которых осуществляется на основании лицензии, не претерпел существенных изменений и по-прежнему порождает ряд вопросов на практике.
Исходя из данных соображений, выбранная проблематика представляется актуальной, имеющей практическое и теоретическое значение, определяет интерес к указанной теме.
Объектом исследования является ввоз лекарственных средств на таможенную территорию ЕАЭС.
Предметом исследования выступают общественно-правовые отношения при осуществлении ввоза лекарственных средств на территорию ЕАЭС, проблемы и пути усовершенствования порядка ввоза лекарственных средств на территорию ЕАЭС.
Целью выпускной квалификационной работы является анализ теоретических и практических аспектов осуществления ввоза лекарственных средств на таможенную территорию ЕАЭС для разработки предложений по совершенствованию процедуры ввоза лекарственных средств.
Достижение поставленной цели требует решения следующих задач:
1) изучить порядок ввоза лекарственных средств на территорию ЕАЭС;
2) изучить таможенный контроль при ввозе лекарственных средств на территорию ЕАЭС;
3) рассмотреть реализацию на практике ввоза на таможенную территорию ЕАЭС лекарств;
4) выявить практические проблемы ввоза на таможенную территорию ЕАЭС лекарств;
5) разработать практические рекомендации по усовершенствованию ввоза лекарственных средств на территорию ЕАЭС.
Теоретической и методологической основой написания выпускной квалификационной работы явились международные соглашения, законодательные и нормативные акты, учебные пособия, монографии и статьи в периодических изданиях по изучаемому вопросу. В работе использовались данные, необходимые для проведенного исследования, из средств массовой информации, включая информацию из компьютерной сети Internet. А также основой проведенного исследования составляют труды российских и зарубежных экономистов, специалистов в области оборота лекарственных средств, теории государственного управления и таможенного регулирования.
Структура работы: введение, три главы, заключение, список литературы, приложения.
Введение раскрывает актуальность, определяет степень научной разработки темы, цель исследования, раскрывает теоретическую и практическую значимость работы.
В первой главе «Правовое регулирование и таможенный контроль ввоза лекарственных средств на территорию ЕАЭС» рассматривается порядок ввоза лекарственных средств на территорию ЕАЭС и процедура таможенного контроля.
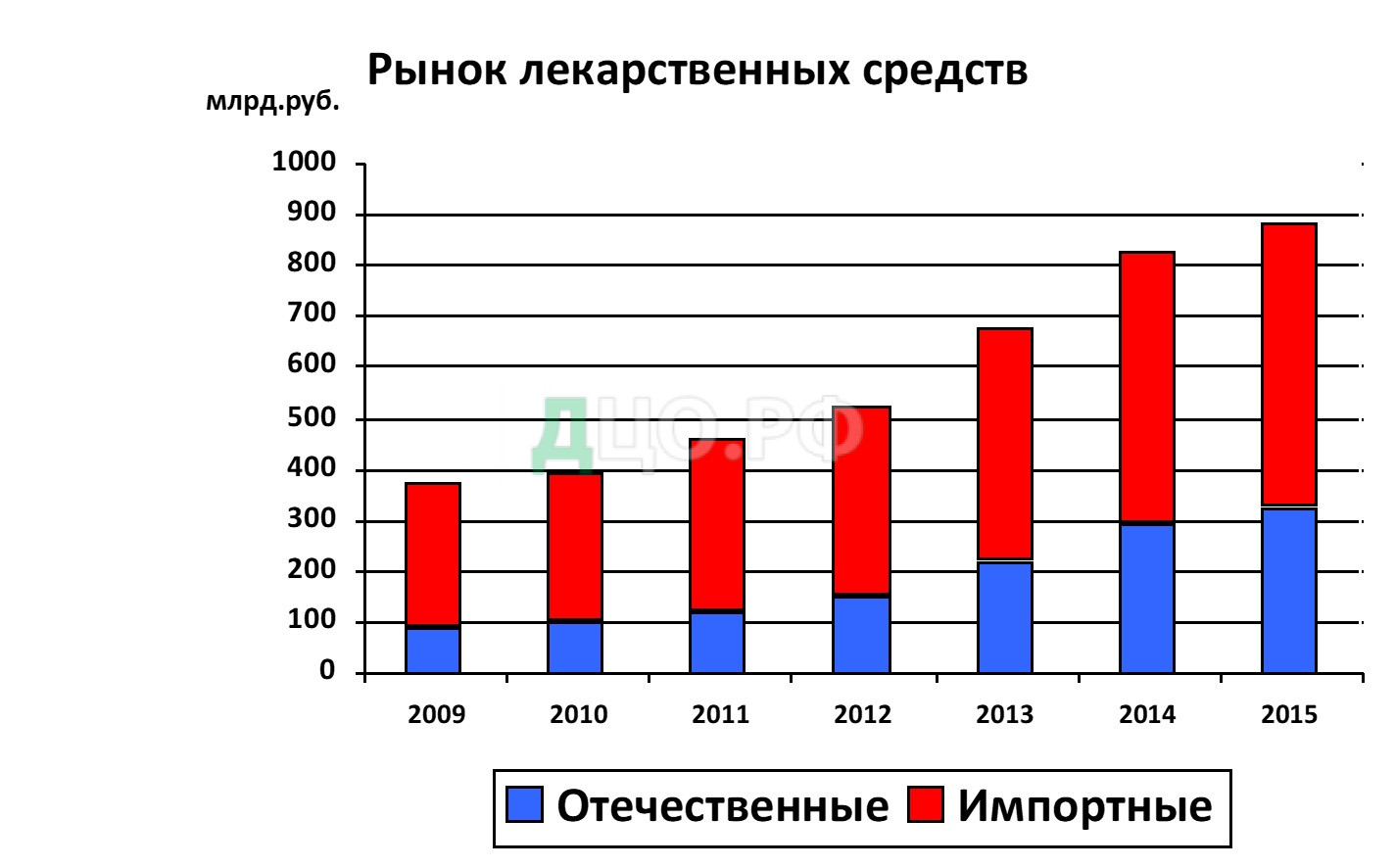
Во второй главе «Порядок ввоза на таможенную территорию ЕАЭС лекарств» проводится анализ состояния рынка лекарственных средств. В данной главе также выявляются проблемы диагностики и идентификации средств при таможенном контроле.
В третьей главе «Совершенствование порядка ввоза на таможенную территорию ЕАЭС лекарственных средств» приводятся практические рекомендации по усовершенствованию ввоза лекарственных средств на территорию ЕАЭС.
В заключении подводятся итоги исследования, формируются окончательные выводы по исследуемой теме, выносятся предложения.
Заключение
Основная деятельность таможенных органов заключается в таможенном контроле над перемещением товаров и транспортных средств через территорию ЕАЭС. Соблюдение законодательства является неизбежным процессом перемещения товаров и транспортных средств через территорию ЕАЭС. Основные принципы перемещения товаров и транспортных средств установлены кодексом ЕАЭС (далее ТК ЕАЭС), действующего с первого января 2016 года, и другими нормативно-правовыми актами. В соответствии со статьей 3 ТК ЕАЭС таможенное законодательство ЕАЭС состоит из ТК ЕАЭС, международных договоров государств — членов ЕАЭС, регулирующих таможенные правоотношения в ЕАЭС, решений Евразийской экономической комиссии, регулирующих таможенные правоотношения в ЕАЭС, принимаемых в соответствии с ТК ЕАЭС и международными договорами государств — членов ЕАЭС.
В области регулирования внешнеэкономической деятельности на фармацевтическом рынке принято значительное количество подзаконных нормативных актов в рамках исполнения Федерального закона «Об обращении лекарственных средств», а также межгосударственных документов в рамках формирования ЕАЭС Армении, Беларуси, Казахстана, Киргизии и России. Лекарственные средства и фармацевтические субстанции включены в единый перечень товаров, к которым применяются запреты или ограничения на ввоз или вывоз государствами — участниками ЕАЭС.
Ввоз лекарственных средств (в том числе незарегистрированных) в некоммерческих целях — физическими лицами для личного пользования, работниками дипломатического корпуса или представителями международных организаций, для лечения пассажиров и членов экипажей или водителей транспортных средств, поездных бригад, для лечения участников международных культурных, спортивных мероприятий и экспедиций осуществляется «без разрешения уполномоченного государственного органа в сфере обращения лекарственных средств». Пассажиры могут свободно вывозить и ввозить через границу ЕАЭС лекарства для личного пользования. Независимо от вида лекарственных средств, должна быть в наличии аннотация к ним, содержащая информацию о составе лекарственного средства и его фармакологических свойствах. Если в состав лекарства входят наркотические средства или психотропные вещества, то путь по «зеленому коридору» закрыт. Если у пассажира в ручной клади или багаже есть лекарства с сильнодействующими (наркотическими, психотропными) веществами, то обязательно нужно задекларировать их в пассажирской декларации.
Любая страна пытается защитить своих национальных производителей, создать условия для экономической безопасности страны, в частности используя тарифные (ставки таможенной пошлины) и нетарифные меры регулирования при ввозе товаров из-за границы. Более 70% реализуемых на территории ЕАЭС лекарственных средств и фармацевтических субстанций в стоимостном выражении иностранные. В ЕАЭС под нетарифными мерами подразумевается государственное вмешательство во внешнюю торговлю, связанное с разрешительным порядком перемещений той или иной категории товаров. Под термин «запреты и ограничения» попадают 7 методов госрегулирования внешней торговли: нетарифные меры (лицензирование, квотирование, разрешительный порядок, в т.ч. в отношении лекарственных средств), меры экспортного контроля, технического регулирования, саниарные меры, ветеринарные меры, фитосанитарные меры и радиационный контроль. Лекарственные средства при ввозе в ЕАЭС попадают под нетарифные меры регулирования. В соответствии с 26-ой статьей Договора о ЕЭАС на териитории России, Казахстана, Беларуси, Армении и Киргизии применяются единые меры регулирования торговли с третьими странами.
В соответствии со ст. 150 ТК ТС все лица на равных основаниях имеют право осуществлять внешнеэкономическую деятельность при выполнении определенных ограничений.
Статья 152 ТК ТС гласит, что при перемещении товаров должны соблюдаться запреты и ограничения. В рамках документов ЕАЭС ограничения при ввозе ЛС и фармацевтических субстанций регламентируются Решением Коллегии Евразийской экономической комиссии от 16.08.12 № 134 (ред. 06.10.15).
В настоящее время сложились противоречия в законодательстве РФ в рамках верхнего законодательства Евразийской экономической комиссии. В ТК предусмотрено, что запрет на ограничения – это меры госрегулирования, которые устанавливаются законодательством ЕАЭС, а также национальными актами, изданными в их развитие. Противоречие в том, что Федеральным законом определен конкретный перечень лиц, которые имеют право на осуществление внешней торговли, на ввоз ЛС: производители, различные учреждения медицинской направленности. В законодательстве ЕАЭС таких норм не установлено.
В федеральном законодательстве есть положение, когда при ввозе ЛС и фармсубстанций должен быть оформлен и предоставляться так называемый сертификат производителя лекарственных средств. Но в законодательстве ЕАЭС такой нормы нет.
В области технического регулирование сложилась сложная ситуация, связанная в т.ч. и с переходом на стандарты GMP. Решение Комиссии ТС от 28.01.11 № 526 определяет 66 категорий товаров, в отношении которых есть возможность установления технических требований. В отношении товаров вне этих категорий предусмотрено, что национальное законодательство не имеет права устанавливать дополнительные требования. ЛС и фармацевтические субстанции не вошли в эти 66 категорий. Но до сих пор продолжается практика предоставления сертификата таможенным органам.
Что касается лекарственных средств, ввозимых в Армению, Казахстан и Кыргызстан, то ставки ввозных пошлин на некоторые лекарственные средства в этих странах ниже, чем предусматривает Единый таможенный тариф ЕАЭС. Армения и Кыргызстан вступили в ЕАЭС с определенными изъятиями в части применения ставок Единого таможенного тарифа (например, Армения начнет применять ЕТТ в отношении лекарственных средств только с 2020 года). Ставки ввозных пошлин в Казахстане на некоторые товарные группы ниже ставок ЕТТ вследствие недавнего вступления страны в ВТО, и Протокол о некоторых вопросах ввоза и обращения товаров на таможенной территории Евразийского экономического союза, который был ратифицирован РФ 30 декабря 2015 года, предусматривает обязательства Казахстана по недопущению реэкспорта из Казахстана товаров, по которым ввозные пошлины ниже ставок ЕТТ
В 2016 году Россия должна ратифицировать Соглашение между странами ЕАЭС об обращении лекарственных средств и медицинских изделий, что обеспечит создание единого фармацевтического рынка ЕАЭС.
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Прикрепленные файлы: |
|
|---|---|

|
Администрация сайта не рекомендует использовать бесплатные работы для сдачи преподавателю. Эти работы могут не пройти проверку на уникальность. Узнайте стоимость уникальной работы, заполните форму ниже: Узнать стоимость |

|
Скачать файлы:
|
Скриншоты работы: |
|
|---|---|
|
|
|