или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Страницы: 1 2
Оглавление
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
- Список сокращений и терминов, используемых в работе.
- Введение.
- Глава 1.ОБЗОР ЛИТЕРАТУРЫ
- 1.1. Общие проблемы антибиотикорезистентности.
- 1.2. Оценка частоты распространения антибиотикорезистентности.
- 1.3. Факторы риска в амбулаторной практике.
- 1.3.1. Золотистый стафилококк и его медицинское значение.
- 1.3.2. Пневмококк и его медицинское значение.
- Глава 2. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ.
- Глава 3. РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ.
- Выводы:
- Список литературы.
Введение
В настоящее время в связи с широким и зачастую неконтролируемым применением антибактериальных препаратов в здравоохранении возникает проблема устойчивости возбудителей инфекционных заболеваний к антибиотикам [78]. Нерациональное использование противомикробных препаратов, способствует появлению и отбору резистентных штаммов, в том числе и к препаратам резерва [33, 75]. Это явление создает огромные сложности в терапии; ведение пациентов с заболеваниями, вызванными устойчивыми к антибиотикам штаммами, влечет за собой все больше экономических и людских затрат [55, 67, 88].
Наиболее распространенной инфекционной патологией детского возраста являются заболевания ЛОР-органов и верхних дыхательных путей: отиты, тонзиллиты, риносинуситы, бронхиты и пневмонии. По данным ВОЗ, от пневмонии ежегодно погибает до 1,8 млн детей младше 5 лет, больше, чем от любой другой болезни. В 2009 году ввиду важности проблемы специалистами ВОЗ и ЮНИСЕФ был декларирован «Глобальный план действий по профилактике пневмонии и борьбе с ней (GAPP)»[80]. Инфекции носоглотки и среднего уха так же составляют значительный вес в патологии детского возраста. Основными возбудителями данных групп заболеваний считаются Staphylococcus aureus, Streptococcus pneumoniae и Haemophylus influenzae [35, 40, 49, 52, 77]. Многочисленные исследования как в Российской Федерации, так и за рубежом демонстрируют рост частоты встречаемости устойчивых к антибиотикам штаммов данных возбудителей, что диктует необходимость коррекции существующих рекомендаций по профилактике и лечению заболеваний, этиологическими факторами которых являются данные микроорганизмы [2, 7, 43].
Для понимания причин возникновения и тенденций распространения резистентности к антибиотикам необходим мониторинг за устойчивостью к антибиотикам, выделенных микроорганизмов, возбудителей инфекций ЛОР-органов и верхних дыхательных путей у детей.[55]
Целью работы является эпидемиологическая оценка потенциальных факторов риска колонизации детей антибиотикорезистентными штаммами основных возбудителей инфекций ЛОР-органов во внебольничных условиях.
Основными задачами настоящей работы явилось следующее:
- установить удельный вес антибиотикорезистентных штаммов Streptococcus spp. и Staphylococcus aureus во внебольничной популяции
- выявить факторы риска колонизации антибиотикорезистентными штаммами Streptococcus spp. и Staphylococcus aureus
- обосновать профилактические и противоэпидемические мероприятия в отношении данной группы инфекций, основываясь на результатах оценки изученных факторов риска.
Объектом исследования являются факторы риска колонизации антибиотикорезистентными штаммами Streptococcus spp. и Staphylococcus aureus.
Предмет исследования: дети, обратившиеся в амбулаторно-поликлинические отделения и отделения стационара.
Положения, выносимые на защиту.
- Среди возбудителей заболеваний ЛОР – органов у детей получили распространение штаммы Streptococcus spp. и Staphylococcus aureus, обладающие устойчивостью к бета-лактамным антибиотикам и антибиотикам группы макролидов.
- Вакцинация пневмококковыми вакцинами является фактором, оказывающим превентивное воздействие на колонизацию антибиотикорезистентными штаммами Streptococcus spp. и Staphylococcus aureus.
Научная новизна исследования.
В настоящем исследовании впервые в России проведена оценка факторов риска носительства штаммов Streptococcus spp. и Staphylococcus aureus., обладающих устойчивостью к антибиотикам, наиболее часто применяемым в клинической практике, во внебольничной популяции детей различного возраста.
Теоретическая и практическая значимость исследования.
Теоретическая значимость силами результатов работы которых заключатся в дополнении имеющихся знаний о влиянии различных биологических и социальных факторов связано на распространенность носительства антибиотикорезистентных штаммов стрептококков и стафилококков, обуславливающих развитие заболеваний ЛОР – органов.
Востребованность результатов настоящего исследования на практике связана с необходимостью совершенствования профилактических мероприятий, направленных на борьбу с распространением резистентности к антимикробным препаратам среди групп населения, наиболее подверженных заболеваниям респираторного тракта и ЛОР – органов – детей дошкольного и школьного возраста.
Полученные результаты работы создают задел для проведения масштабных эпидемиологических исследований, направленных на выявление групп риска в отношение состояния колонизации антибиотикорезистентными возбудителями в негоспитальных условиях.
Дизайн и методы исследования. В качестве дизайна исследования для выявления потенциальных факторов риска был выбран дизайн – «случай-контроль». Принципы формирования базы исследования представлены на рисунке 1.
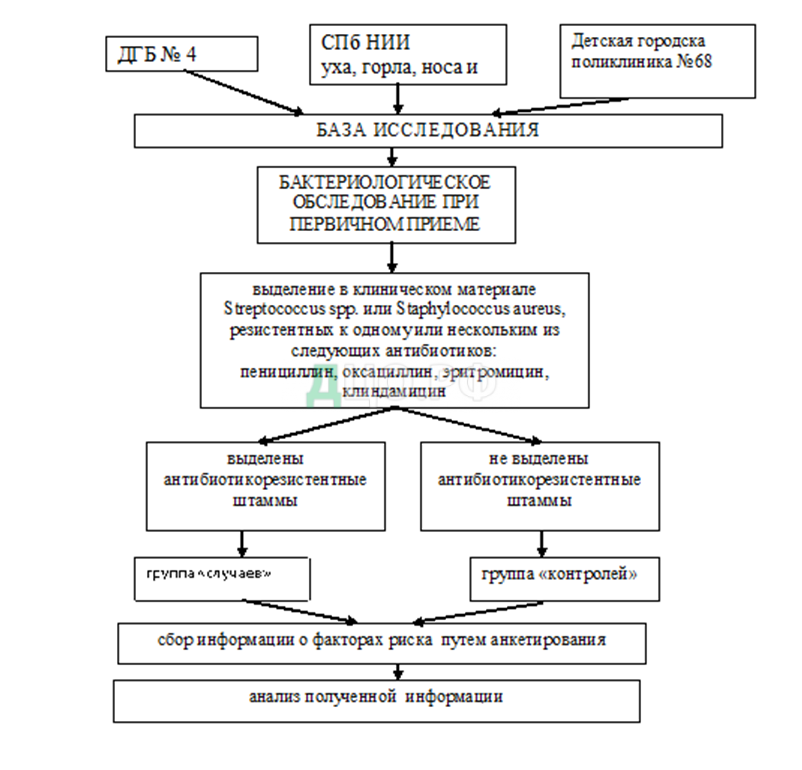
Сбор информации осуществлялся наиболее доступным способом – посредствам анкет-опросников, заполняемыми родителями детей, включенных в исследование.
Внедрение результатов исследования. Результаты работы могут быть использованы при разработке методических рекомендаций для врачей-эпидемиологов, батериологов, педиатров, разрабатываемых кафедрой эпидемиологии, паразитологии и дезинфектологии СЗГМУ им. И.И. Мечникова. Материалы работы будут использованы в учебном процессе.
Структура и объем диссертации.
Диссертационная работа состоит из введения, обзора литературы, материалов и методов, главы результатов собственных исследований и их обсуждения, выводов и списка цитируемой литературы. Работа изложена на 55 страницах машинописного текста, содержит 6 таблиц, 3 рисунка. В работе использованы 29 отечественных и 59 иностранных источников литературы.
Глава 1 ОБЗОР ЛИТЕРАТУРЫ
1.1. Общие проблемы антибиотикорезистентности
Проблема роста устойчивости возбудителей внебольничных и нозокомиальных инфекций к антибактериальным препаратам в настоящее время приобретает глобальный характер. На решении этого вопроса сосредоточены усилия микробиологов, исследователей — клиницистов, а также специалистов в области организации здравоохранения. В повседневной клинической практике врач, практически любой специальности, сталкивается с трудностью лечения инфекционно — воспалительных заболеваний, вызванных полирезистентными штаммами микроорганизмов, традиционными схемами лечения, соответствующими общепринятыми методами [23].
Разработка противомикробных препаратов, особенно антибиотиков, сыграла значительную роль в существенном снижении заболеваемости и смертности многих инфекционных заболеваний. Однако тот факт, что бактерии могут развивать устойчивость к антибиотикам, привел к тому, что антимикробные агенты теряют свою эффективность из-за распространения и стойкости лекарственно-устойчивых организмов. Для борьбы с этим необходимо разрабатывать все более и более новые антибиотики с повышенным терапевтическим и профилактическим действием. Эта глава посвящена устойчивости к антибиотикам у бактерий, которые являются патогенными для человека. Значительная озабоченность вызывает нерациональное и бесконтрольное использование антибиотиков. Установлено, что устойчивость к антибиотикам у патогенных организмов широко объясняется «неправильным использованием» антибиотиков для лечения и профилактики заболеваний, что приводит к накоплению устойчивых бактерий во флоре [40, 41, 43, 46, 50, 87].
Открытие антибиотиков стало поворотной точкой в истории человечества. Тем не менее, к концу 1950-х годов сообщалось об инфекциях, которые трудно поддавались лечению, включая резистентные бактерии. В настоящее время мультирезистентные штаммы стали серьезной проблемой для здоровья населения и животных. Противомикробная резистентность — сложная проблема, связанная со способностью бактерий быстро адаптироваться к окружающей среде. Антибиотики и резистентные к антибиотикам бактерии и детерминанты существовали до открытия и использования людьми антибиотиков. Устойчивость к антимикробным агентам — это инструмент, который позволяет бактериям выживать в окружающей среде и развиваться. Гены устойчивости могут передаваться между бактериями горизонтальным переносом, включающим три механизма: конъюгацию, трансдукцию и трансформацию[70]. Устойчивые бактерии могут возникать в любом месте, когда развиваются соответствующие условия. Антибиотики представляют собой мощный селектор для устойчивости к противомикробным препаратам у бактерий. Сокращение использования противомикробных препаратов является одним из способов контроля устойчивости к противомикробным препаратам; Однако для достижения этой цели необходимо осуществить полный комплекс мер[30, 38].
Большинство бактериальных инфекций являются важной и интересной проблемой в организации здравоохранения, в тоже время их лечение представляют определенные сложности. С одной стороны, при этих заболеваниях может быть достигнуто радикальное излечение больного, в отличие от многих других, неинфекционных заболеваний. С другой стороны, инфекционное заболевание представляет собой сложный, динамический процесс, обусловленный особенностями микроорганизмов и макроорганизма, в результате чего невозможно представить абсолютные рекомендации по лечению конкретных нозологических форм у различных больных [2, 4, 5]. Подходы к лечению одного и того же заболевания могут изменяться в зависимости от страны, региона, лечебного учреждения и лечебного отделения, а также в зависимости от возраста больных, сопутствующих заболеваний и т. д. Впервые антибиотические свойства зеленой плесени были открыты Л. Флемингом в 1928 г., и позднее в период Первой Мировой войны они послужили основанием для выделения антибиотиков в чистом виде группой английских химиков: Н. Flori, Е. Chain, Е. Abraham в Оксфорде [7, 20, 31]. В нашей стране впервые пенициллин выделен из другого вида плесени — Penicillium crustosum З.В. Ермольевой [7]. С этой поры началась эра антибиотикотерапии. Апробация пенициллина показала, что он является мощным средством профилактики и лечения гнойной инфекции. Далее появились новые антибиотики, получившие всемирное признание и длительное время наблюдался небывалый оптимизм в отношении их антибактериальных возможностей. Успехи антибактериальной терапии, программ вакцинации, возможность синтеза новых антибактериальных препаратов, обеспечение населения качественной водой и продуктами питания создали в конце 60-х годов иллюзию близкой и окончательной победы над инфекционными заболеваниями [1,4,16,]. Однако широкое повсеместное и часто бесконтрольное применение антибактериальных препаратов привело к возникновению уже к концу 70-х годов сложных проблем. В значительной степени изменился видовой состав микрофлоры в сторону преобладания стафилококковой и условно-патогенной флоры, которая приобрела высоковирулентные свойства, стрептококковая инфекция постепенно отходила на второй план, уступая место грамотрицательной флоре. Мир столкнулся с проблемой резистентности микроорганизмов к антибактериальным препаратам, что вызвало необходимость массивного применения антибиотиков, увеличения дозировок, частой смены препаратов, поиска новых групп препаратов. Все это привело к формированию новых антибиотикорезистентных штаммов микроорганизмов, таким образом, порочный круг замкнулся [57, 58, 60, 66]. В настоящее время летальность от антибиотикорезистентных инфекций достигает уровня доантибиотиковой эры, и теперь уже очевидно, что основными причинами этого явления явились изменение характера патогенной микрофлоры с прогрессивно нарастающей устойчивостью её к антибиотикам, иммуносупрессия, дисбактериозы, а также необоснованные назначения и прием, которые привели к заметному снижению их эффективности.
Неуклонный рост числа инфекционных заболеваний и гнойновоспалительных осложнений в клинике ставит проблемы антибиотикотерапии на одно из первых мест в системе медикаментозного лечения. В настоящее время в мировом здравоохранении накоплено большое число данных о многих известных заболеваний и выявлены их связи с различными микроорганизмами. Современные достижения в области этиотропной антибактериальной химиотерапии основаны на развитии идей Пауля Эрлиха о возможности создания веществ, избирательно подавляющих жизнедеятельность микроорганизмов, но практически не влияющих на функции организма человека («золотые пули Эрлиха»)[7]. Сложности антибактериальной терапии, прежде всего, связаны с разнообразием возбудителей заболеваний, их различной чувствительностью и резистентностью к лекарственным препаратам, даже в пределах одного вида бактерий и их частой сменяемостью, состоянием макроорганизма (иммунный статус, возраст, сопутствующие заболевания), трудностью выявления и идентификации патогенных микроорганизмов, частым возникновением смешанных инфекций и т.д.[3,17,32]. Существенной проблемой также является дифференциация бактериального и вирусного заболевания. В тоже время для заболеваний, где бактериальная этиология уже не вызывает сомнении, постоянно возрастает актуальность повышения эффективности диагностики, лечения и предотвращения распространенности антибиотикорезистентных форм. Решение этих проблем во всем мире считается одним из приоритетных вопросов на пути к увеличению продолжительности и качества жизни людей в большинстве стран регулируется на законодательном уровне[7]. В странах с ограниченным финансированием здравоохранения cиcтематическое наблюдение за развитием антибиотикорезистентных штаммов имеет низкий приоритет, что в свою очередь не позволяет в должной мере выполнять стандарты качества оказания медицинской помощи населению. В этих странах такие проблемы, как высокий показатель инфекционной заболеваемости, распространение устойчивых к антибиотикам штаммов микроорганизмов, трудно поддающихся лечению доступными антибиотиками, а также отсутствие соответствующего эпидемиологического надзора сочетаются с переполненностью стационаров, неблагоприятной эпидемиологической обстановкой, частым развитием инфекционных осложнений[14, 15, 21].
Грамотная этиологическая диагностика необходима для обоснованного выбора антимикробной терапии, наиболее адекватных природе выделенного возбудителя, либо ассоциации инфекционных агентов. Арсенал антибиотиков и химиотерапевтических препаратов постоянно расширяется и обновляется в связи с неуклонным ростом резистентности микрофлоры, обусловленной во многом нерациональным их применением[25, 26, 86, 83]. Нерациональное назначение антибиотиков приводит к формированию лекарственной устойчивости микроорганизмов, селекции особо вирулентных госпитальных штаммов, борьба с которыми чрезвычайно затруднена. При этом происходит не только снижение эффективности лечения, но и изменение нормальной микрофлоры организма, её естественной антагонистической активности, что облегчает проникновение в организм больного патогенного возбудителя. Ряд авторов полагают, что нормальная микрофлора человека и животных является резервуаром широкого распространения устойчивых патогенных форм[61, 72, 73]. Благодаря обилию и разнообразию транзиторных микроорганизмов, представителей нормальной микрофлоры, а также условий, способствующих широкому и быстрому переносу бактериальных генов как от предшествующих поколений микроорганизмов последующим, так и через границы видов, родов и семейств, процесс образования или селекции антибиотикоустойчивых штаммов микроорганизмов происходит на протяжении относительно короткого периода времени[7]. Своевременная и рациональная антибиотикотерапия является исключительно важным фактором, лимитирующим как появление осложнений, так и хронизацию процесса. Целенаправленная этиотропная терапия предполагает назначение препарата активного против микроорганизма, вызвавшего заболевание в конкретном случае. Однако, микробиологическое исследование требует определенного времени, а так как назначение антибактериального препарата необходимо при первом обращении больного к врачу, в подавляющем большинстве случаев выбор антибиотика происходит эмпирически[6, 19, 69]. В свою очередь, эмпирический подход должен базироваться на представлениях о спектре основных возбудителей и их чувствительности к антибиотикам, на клинической эффективности различных групп антибактериальных препаратов, подтвержденной в динамических клинических исследованиях . Успех антибактериальной терапии зависит не только от появления новых, более эффективных препаратов, но и с рациональным использованием их, что зависит от применения антибиотиков с учетом показаний и противопоказаний, особенностей фармакокинетики, побочного действия, правильности дозирования и взаимодействия между собой и с другими лекарственными средствами, ориентировки в вопросах микробиологии, клинической фармакологии, эпидемиологии. Пренебрежение к одному из перечисленных правил терапии антибиотиками ведет к большому числу ошибок, снижающих успех терапии. Согласно И.В. Давыдовскому, «врачебные ошибки — род добросовестных заблужденийврача в его суждениях и действиях при исполнении им тех или иных специальных врачебных обязанностей»[7]. Ошибки в антибактериальной терапии имеют не только чисто медицинские, но и различные социальные, деонтологические, экономические и другие аспекты. Наиболее неблагоприятным аспектом является формирование антибиотикорезистентных штаммов микроорганизмов. Резистентность к антибиотикам — своеобразное социально-биологическое явление эволюции микроорганизмов, возникшее в результате использования этих препаратов, мутационного процесса, обмена R- плазмидами, несущими информацию о резистентности и селективного отбора в популяции. Теоретическое и практическое значение этого явления осмысленно недостаточно. Появление резистентных бактерий — динамический процесс, происходящий во всем мире и требующий постоянного многопланового изучения[8, 28, 34]. До настоящего времени большинство врачей получают очень скудную информацию о свойствах микроорганизмов, которые циркулируют в их регионе. Как результат, доступные показатели только частично помогают в выборе эффективной антибиотикотерапии. Вместе с тем, в работах многих научных центров показано, что чувствительность к антибиотикам имеет индивидуальный характер даже у бактерий, циркулирующих в разных регионах, разных лечебных учреждениях и т.д. Чувствительность к антибиотикам микробов, выделенных на разных территориях, зависит от многих причин[7]. Прежде всего, она отражает историю применения тех или иных препаратов, использование антибиотиков для самолечения, качество диагностики, квалификацию врачей, назначающих антибиотикотерапию, число больных в стационарах и др. Таким образом, имеющиеся литературные данные позволяют проследить только тенденцию изменения чувствительности бактерий, но не дают представлений об их свойствах в каждом отдельном регионе. Очевидно, что в лечебных учреждениях при интенсивном и частом применении антибиотиков у пациентов, находящихся в ограниченном пространстве, условия для формирования и распространения антибиотикорезистентности значительно более благоприятны, чем в любом другом месте. Проблема антибиотикорезистентности в стационаре любого профиля напрямую связана с формированием госпитальных штаммов микроорганизмов[7,9]. Адаптация госпитального штамма к условиям определенного стационара приводит к тому, что вне сложившейся экологической системы он оказывается маложизнеспособным. Формированию госпитальных штаммов способствуют и многие внебольничные факторы современной жизни. Широкое применение антибиотиков не только в медицине, но и в ветеринарии, животноводстве, сельском хозяйстве, пищевой промышленности создает условия для эволюционных изменений микроорганизмов, которые выражаются в формировании полирезистентности к антибактериальным препаратам, повышении вирулентности патогенных микроорганизмов, появлении вирулентных условно-патогенных микроорганизмов и даже приобретении патогенности микроорганизмами, ранее считавшимися облигатными сапрофитами человека[37,42]. Необходимо отметить, что термин условно-патогенный микроорганизм весьма условен, так как вряд ли возможно провести четкие границы, отличающие этих возбудителей от облигатно-патогенных бактерий. По видимому, эта неопределенность кроется в условиях обитания конкретных микроорганизмов. В настоящее время описан целый ряд факторов, которые при определенных условиях могут обеспечивать патогенное действие на макроорганизм: поверхностные структуры, ответственные за прикрепление к эпителиальным клеткам, различные внеклеточные продукты типа экзотоксинов, ферменты патогенности, главным образом обладающие инвазивной активностью, эндотоксин, а также факторы, обуславливающие селективные преимущества (устойчивость к антибактериальным препаратам, продукция бактерицинов и др.)[10,18,24,54]. Подобными свойствами обладают госпитальные эковары условно-патогенных микроорганизмов, которые на основании их вирулентных свойств и определенного набора факторов; патогенности; максимально приближены к облигатно-патогенным микроорганизмам, по сравнению с внебольничными эковарами (штаммами, обладающими типичными для определенного вида свойствами, вне зависимости от места их выделения). Усиление патогенных свойств условно-патогенной микрофлоры в значительной степени обусловлено нерациональным применением антибиотиков, что неминуемо приводит к развитию антибиотикорезистентных штаммов микроорганизмов[7]. Определенную роль в развитии антибиотикорезистентности в современных условиях играет также общее снижение резистентности макроорганизма, связанное с экологическим неблагополучием, химическим загрязнением атмосферы, развитии транспортных связей, высоким уровнем миграции населения, хроническими стрессами, распространением алкоголизма, наркомании и др [7,74,68,58]
1.2. Оценка частоты распространения антибиотикорезистентности
Поскольку систематических исследований распространенности внебольничных MRSA в России, как и в других странах, не проводилось, сложно оценить истинные масштабы явления. По данным метаанализа, включавшего оценку 27 ретроспективных и 5 проспективных исследований, доля внебольничных штаммов MRSA среди всех резистентных штаммов, выделенных у госпитализированных пациентов на территории США, составила 30,2% (с колебаниями в пределах 1,9–96%) и 37,3% (18,2–51,2%) соответственно. Частота носительства MRSA во внебольничных условиях составила 1,3% (95% доверительный интервал 1,04–1,53%), однако исследуемые группы значительно отличались друг от друга [40]. Представлены основные тенденции в развитии резистентности к пенициллину и метициллину (оксациллину) среди нозокомиальных и внебольничных штаммов S. aureus. Резистентность S. aureus к пенициллину, изначально возникшая в условиях лечебных учреждений, впоследствии получила широкое распространение за их пределами, практически достигнув уровня, характерного для нозокомиальных изолятов. Вполне вероятно, что в ближайшие годы подобная тенденция будет наблюдаться и по отношению к MRSA, учитывая рост частоты их выявления, как в лечебных учреждениях, так и амбулаторно [26,84].
Устойчивость к противомикробным препаратам (AMR) представляет серьезную угрозу общественному здоровью также и в Европе, что приводит к увеличению расходов на здравоохранение, неудач лечения и смертности. Анализы Европейского центра по профилактике и контролю заболеваний (ECDC) подсчитали, что инфекции, вызванные поднабором лекарственно-устойчивых бактерий, ежегодно приводят к гибели около 25 000 человек в Европе. В дополнение к этим предотвратимым смертельным исходам это также приводит к дополнительным расходам на здравоохранение и снижению производительности как минимум на 1,5 млрд. Евро [71,72].
Этот вопрос требует согласованных усилий на уровне государств-членов, а также тесного международного сотрудничества в целях сохранения в будущем антимикробной эффективности и доступа к эффективному лечению бактериальных инфекций. В 2008 году Европейский совет принял выводы, призывающие Европейскую комиссию содействовать сотрудничеству между Комиссией, агентствами и государствами-членами в борьбе с AMR [47]. В Плане действий, изданном Комиссией в 2011 году, надзор за AMR указывается как одна из областей, где наиболее необходимы меры, наряду с надлежащим использованием противомикробных препаратов, профилактикой и борьбой с инфекциями и разработкой новых эффективных противомикробных препаратов или альтернатив для Лечение [68,72,81,82].
Первое сообщение о выделении резистентного к пенициллину ПК было получено из Австралии в 1967 году. В 1974 году появилось сообщение о первом пенициллинорезистентном пневмококке в США, выделенном у ребенка с серповидноклеточной анемией и пневмококковым менингитом. Европейскими «мекками» антибиотикорезистентности в настоящее время являются Испания и Венгрия [80]. В Испании 2/3 всех штаммов пневмококков резистентны как минимум к одному антибиотику. В Венгрии 70% резистентных штаммов ПК, выделенных у детей, являются мультирезистентными, из них половина — высокорезистентными. Были обнаружены чрезвычайно высокие показатели резистентности к тетрациклину- 90%, эритромицину — 70%, ко-тримоксазолу — 65% [77]. В исследовании более чем 1500 изолятов S.pneumoniae, взятых у амбулаторных больных медицинских центров США в 1994-1995 гг., 23,6% изолятов были не чувствительны к пенициллину: 14,1% из них характеризовались умеренной устойчивостью, 9,5% — высокой. Во Франции 12% штаммов пенициллинорезистентны, из них половина — высокорезистентны. В Германии умеренно резистентные штаммы наблюдались уже в 80-е годы с частотой выделения 1,7-7%; некоторые из этих штаммов были также резистентны к тетрациклину,хлорамфениколуи другим антибиотикам, то есть были мультирезистентными. Cообщается о штаммах ПК, на которые не действуют цефалоспорины третьего поколения.
Распространению устойчивых ПК способствовало массовое предшествующее применение беталактамных антибиотиков (в 50% случаев). В Южной Африке в богатых районах имеется большая эритромицино- и ко-тримоксазолорезистентность, а в бедных преобладает пенициллинорезистентность в связи с меньшей стоимостью пенициллина по сравнению с другими препаратами. Во Франции уровень эритромицинорезистентности выше, чем в соседней Испании, в связи с более частым применением макролидов [42].
Антибиотикорезистентность представляет собой в настоящее время серьезную проблему медицины, причем в последние 10–15 лет мы констатируем существенный скачок уровня устойчивости практически всех клинических значимых микроорганизмов, вызывающих инфекционные заболевания у человека, а также распространение устойчивых микробов во всех регионах мира. То есть можно говорить о глобализации антибиотикорезистентности и угрозе наступления «постантибиотической» эры, когда инфекционные заболевания вновь могут стать неизлечимыми. Именно так обозначили проблему эксперты Всемирной организации здравоохранения (ВОЗ) в основополагающем документе 2014 года. Эксперты ВОЗ также предупреждают врачей о реальных проблемах устойчивости внебольничных возбудителей. Среди последних следует отметить S. pneumoniae. Причем по медицинскому и социальному значению на первое место справедливо поставлен именно S.pneumoniae[40].
1.3. Факторы риска в амбулаторной практике
Резистентность возбудителей инфекционных заболеваний к антибиотикам является возрастающей проблемой в медицине, и особенно в педиатрии. Эффективность многих антибактериальных препаратов, традиционно используемых для лечения инфекционных болезней у детей, снижается из-за возрастающего распространения устойчивых штаммов бактерий. С генетических позиций устойчивость к антибиотикам может быть природной (как наследуемый видовой признак) или приобретенной . Природная устойчивость ясна для клинициста из характеристики спектра действия антибиотика и легко учитывается при выборе адекватного препарата, в то время как для выявления приобретенной устойчивости требуется лабораторный контроль конкретного штамма.
Традиционно внебольничные вспышки инфекций, вызванные нозокомиальными штаммами MRSA, ассоциируются с факторами риска, которые хорошо известны и включают [18,34, 41]:
- недавнее пребывание в хирургических стационарах и отделениях интенсивной терапии;
- длительное нахождение в стационаре;
- близкий контакт с пациентами, колонизированными или инфицированными MRSA;
- предшествующую антибиотикотерапию;
- ожоги, хирургические раны;
- нахождение на гемодиализе или при хроническом перитонеальном диализе;
- катетеризацию центральных вен;
- пожилой возраст;
- иммунодефицитные состояния.
В отличие от нозокомиальных MRSA, факторы риска инфицирования внебольничными MRSA четко не определены. Как правило, они диагностируются у практически здоровых лиц, однако сравнение сообщений о вспышках инфекции позволило выявить некоторые предрасполагающие к их развитию состояния, такие как [43,79]:
- социальные факторы;
- несоблюдение правил личной гигиены;
- наличие травм кожных покровов;
- детский возраст.
Инфицирование происходит преимущественно контактным путем: либо при прямом контакте с инфицированным лицом, либо с контаминированными предметами. Описаны внутрисемейные случаи распространения инфекции. Большую роль в передаче возбудителя могут играть постельное белье, полотенца и другие средства личной гигиены, а также контаминированный перевязочный материал.
Исходя из вышеизложенного, в группу риска развития заболеваний, вызванных внебольничными MRSA, чаще всего входят дети, спортсмены, работники физического труда, военнослужащие, лица, имеющие татуировки, пирсинг и т.п. [74].
Дети являются одной из основных групп риска.У них чаще выявляется колонизация кожных покровов S. aureus, что связано с особенностями строения кожи, нарушением правил гигиены, а у маленьких детей – с частым контактом с выделениями слизистой оболочки полости носа [62]. По данным проведенного в Чикаго проспективного исследования, в котором приняли участие 500 детей в возрасте до 16 лет, колонизация кожных покровов и слизистой оболочки полости носа метициллино чувствительными штаммами S. aureus достигала 24,4%, MRSA – 2,5% [15]. В Чикаго было выявлено 25 кратное увеличение числа детей, поступивших в стационары по поводу инфекций, вызванных MRSA в амбулаторных условиях [46]. Причем, как в первом, так и во втором исследовании, ни у одного ребенка в анамнезе не было выявлено факторов риска инфицирования нозокомиальными патогенами.
Второй по значимости группой риска являются спортсмены, особенно занимающиеся контактными видами спорта. Для них характерны групповые заболевания, связанные с использованием общего спортивного инвентаря и полотенец, а также частым возникновением травм кожи [36].
1.3.1. Золотистый стафилококк и его медицинское значение
Золотистый стафилококк был впервые обнаружен шотландцем Александром Огстоном в 1880 году в гное из абсцесса [33], и с этого момента знания о его роли в инфекционной патологии постоянно пополнялись. В настоящее время Staphylococcus aureus считается одним из самых частых возбудителей инфекционных заболеваний человека — им колонизировано до трети населения. На уровень колонизации влияет множество факторов, в первую очередь следует обратить внимание на возраст. Частота колонизации детей выше, чем взрослых, особенно у новорожденных; в течение первого года жизни она прогрессивно снижается [35]. Из так называемых факторов хозяина следует отметить так же пол, этнические особенности, иммунный статус, сопутствующие патологии и особенности образа жизни . Кроме того, есть ряд микробных факторов, влияющих на колонизацию стафилококком главного локуса — носоглотки. Это, в первую очередь, взаимодействия различных бактериальных популляций в составе микробиома носоглоточной. Так, показано антагонистическое влияние на культуру золотистого стафилококка пневмококков и некоторых коагулазонегативных стафилококков (S. epidermidis и S. Lugdunensis) [63].
Основными сайтами для колонизации Staphylococcus aureus являются носоглотка, руки и паховая область. Большое значение отводится так же фекальному носительству, которое играет определенную роль в циркуляции возбудителя внутри и вне лечебных учреждений[15]. Так, по данным мета-анализа, уровень фекального носительства прогрессивно увеличивается с 10 до 65% в течение первых 8 недель жизни, затем снижается до 46% к первому году. Общий уровень носительства по данным проанализированных 26 исследований составил 26% (95% ДИ: 16,8-36,3%), носительство метициллинрезситентных штаммов — 10 % (95% ДИ: 0,7-27,0%). Оно может иметь постоянный или транзиторный характер, что подтверждается с помощью бактериологических имолекулярно-генетических методов [88].
Наиболее частыми заболеваниями, вызываемыми данным микроорганизмом, являются пневмонии, бактериемии, инфекции кожи и мягких тканей, эндокардиты, инфекции имплантов и протезов и прочее. Многоцентровое исследование, проводившееся в 2000-2008 годах, выявило отсутствие роста заболеваемости бактериемиями за период исследования и увеличение доли метициллин-резистентных стафилококков; инцидентность бактериемий варьировала от 10 до 30 на 100000 пациенто-лет [42]. В многолетнем исследовании бактериемий в Дании с 1957 по 1990 годы был обнаружен рост заболеваемости с 3 до 20 на 100000 пациенто-лет [40]. Таким образом, можно говорить о стабилизации заболеваемости в последние десятилетия, однако имеют место существенные исзменения в структуре антибиотикорезистетности — доля MRSA увеличивается. Что касается инфекций кожи мягких тканей, то золотистый стафилококк является их основным возбудителем.
Основными факторами вирулентности стафилококков являются:
- PVL-токсин — лейкоцидин Пантона-Валентайна, играющий важную роль в инфекций кожи и мягких тканей и несколько менее значимую — в патогенезе пневмонии, бактериемии и поражении скелетной и мышечной ткани [54]
- протеин А, являющийсия важным фактором защиты от фагоцитоза, а так же выполняющий роль активатора воспалительных реакций в дыхательных путях. Вариации структуры этого белка используются для типирования стафилококков (spa-сиквенс типирование)
- стафилококковые хромосомные кассеты SCCmec,являющиеся сложными генетическими элементами, несущими гены устойчивости к антибиотикам, в первую очередь ген устойчивости к метициллину mecA.
Наличие лейкоцидина Пантона-Валентайна обычно характерно для CO-MRSA и практически не встречается среди госпитальных штаммов. Другим важным критерием, позволяющим определить источник микроорганизма, является тип SCCmec кассеты. Иерархическая система классификации хромосомных кассет mec предполагает выделение их типов (в зависимости от типа генного комлекса ccr и класса гена mec) и подтипов (в зависимости от различных вариаций J-регионов). Генный комплекс ccr состоит из собственно гена ccr, кодирующего фермент рекомбиназу, участвующую в сайт-специфической интеграции кассеты, и окружающих его открытых рамок считывания (open reading frames (ORFs)) с неустановленной на данный момент функцией. Генный комплекс mec состоит из гена mecA, регуляторных генов и связанных с ним инерционных последовательностей. Необязательные элементы SCCmec объединяются в три так называемых J-региона (joining regions); туда могут входит гены резистентности к другим группам антибактериальных препаратов. На сегодняшний день описано 8 типов и 10 подтипов стафилококковых хромосомных кассет SCCmec (см. Рисунок 2). Встречаются также кассеты, не несущие в своем составе гена устойчивости к метициллину, но имеющие детерминанты резистентности к другим антимикробным препаратам, например, к фузидиевой кислоте.
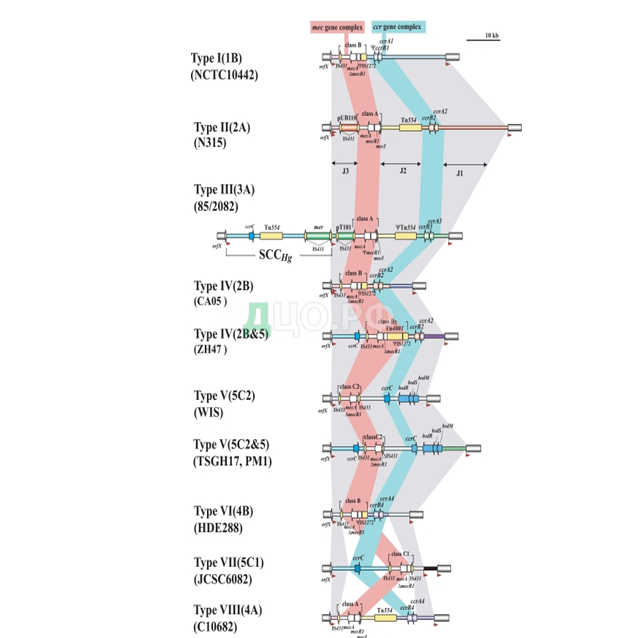
Еще в 1897 году французский врач Эрнест Дюшен отметил свойство некоторых плесневых грибков подавлять рост микроорганизмов [2, 78], однако, заслуга открытия первого антибиотика — пенициллина, полученного из плесени рода Penicillium, принадлежит английскому ученому Александру Флемингу в 1929 году. С изобретением пенициллина удалось значительно снизить частоту раневых инфекций, что было значительным успехом в медицине. Так продолжалось до 1950х годов, когда появились сообщения о стафилококках, синтезирующих пенициллиназы. С появлением полусинтетических антистафилококковых пенициллинов удалось справиться и с этой проблемой, однако, уже в 1961 году, спустя год после внедрения в клиническую практику метициллина, появилась информация о выделении штамма, резистентного к нему [69], а в 1968 году случилась вспышка в Бостонской больнице, вызванная подобными штаммами.
В дальнейшем наблюдался рост частоты выделения метициллинрезистентных штаммов во всем мире, в том числе и в России [19,22]. Резистентность к метициллину — важная проблема терапии стафилококковых инфекций на современном этапе, поскольку имеющие такой тип устойчивости изоляты не поддаются терапии любыми беталактамными антибиотиками, в том числе и защищенными ингибиторами беталактамаз, поскольку механизм устойчивости кроется в мутации пенициллинсвязывающего белка ПСБ2а. Кроме того, метициллинорезистентность может быть сопряжена с устойчивостью к другим АМП. В таком случае препаратом ыбора обычно становиться ванкомицин, но в последнее время отмечается появление устойчивость и к нему — так называемые VRSA, vancomicin resistant Staphylococcus aureus.
По месту возникновения инфекции, вызванные метициллинрезистентными стафилококками, подразделяются на внебольничные и госпитальные. Первоначально случаи инфекции, вызванной MRSA, во внебольничной популяции рассматривались как заносы из стационаров, однако, как стало позже понятно, зачастую источником метициллинрезистентных штаммов становится сама внебольничная популяция [85]. С учетом этого D. Salgado и соавт.[74] предложили выделить помимо нозокомиальных (в случае развития инфекции спустя 48 часов после прибывания в стационар) и истинно внебольничных (community acquired MRSA, CA-MRSA) также community onset MRSA (CO-MRSA, штаммы, вызвавшие инфекции вне стационара), которые, в свою очередь, могут быть получены от пациентов с одним и более фактором риска инфицирования нозокомиальными штаммами или без таковых; применение термина community acquired MRSA (CA-MRSA) для обозначения внебольничных штаммов они считает менее правильным. Принципиально важные различия между госпитальными и внебольничными инфекциями, вызванными MRSA, лежат не только в месте возникновения заболевания (в стенах лечебного учреждения или за его пределами), но и в факторах риска возникновения последних. Для внутрибольничных инфекций важную роль играет характерный антибактериальный анамнез, оперативные вмешательства, проведение гемодиализа, наличие хронических заболевании. По данным S. Fritz и соавт. [44,45], с колонизацией MRSA во внебольничных условиях ассоциированы следующие факторы: ежедневный прием лекарств, антибактериальная терапия, оперативные вмешательства и посещение учреждений здравоохранения в течение года, системные инфекции в анамнезе, работа членов семьи в сфере здравоохранения, домашние животные, проживание членов семьи старше 60 лет, скученность семьи, низкие социально-бытовые условия, занятия спортом[18].
Для внебольничного стафилококка характерна клональная структура распространения, при которой на определенной территории циркулируе одна или несколько ведущих клональных линий. Для выявления этого свойства используются различные молекулярно-генетические методы типирования: spa-сиквенстипирование, многолокусное сиквенстипирование (MLST) по выявлению вариабельности в семи генах домашнего хозяйства — определение ST-типа, электрофорез в пульсирующем поле (PFGE) и определение типа SCCmec кассеты [11,56]. По литературным данным, наиболее часто встречающимися в мире госпитальными MRSA является клональная линия ST239, например, ST239/SCCmecIIIA и ST239/SCCmecIII, а так же ST5, к примеру, ST5/SCCmecII [33].
Для внебольничных штаммов характерны сиквенс-типы ST8/SCCmecIVa (USA300), ST30/SCCmecIV, ST59/SCCmecV и ST80/SCCmecIV [33]. Так, к примеру, на территории США в течение последних лет ведущим является USA300, сменивший в начале 2000-х циркулировавший до этого клон USA400, характеризующийся помимо высокой устойчивости к антибактериальным препаратам повышенной частотой встречаемости редких генов патогенности [47]. В Германии в качестве ведущего госпитального клона был идентифицирован ST22, из негоспитальных штаммов MRSA преобладали относившиеся к ST398, а также к CC1, CC9 и CC398, характерные для остальных Европейских стран. Встречамость факторов вирулентности коррелировала с клональной структурой [45]. На формирование пандемических клонов большое влияние также оказывают миграционные процессы [59].
Таким образом, на распространение метициллинрезистентных стафилококков влияет множество факторов. Для более глубокого понимания мехнизмов и путей развития эпидемического процесса необходимо проведение качественных эпидемиологических исследований.
Страницы: 1 2
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
