или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
1.6. Характеристики сырья
1.6.1. Лигнин
Лигнин (от лат. lignum — дерево, древесина) — сложный, сетчатый природный ароматический полимер, входящий в состав наземных растений. Характеризует одеревеневшие стенки растительных клеток. Является продуктом биосинтеза. Содержится в клетках сосудистых растений и некоторых водорослях. Одеревеневшие клеточные оболочки обладают ультраструктурой, которую можно сравнить со структурой железобетона: микрофибриллы целлюлозы по своим свойствам соответствуют арматуре, а лигнин, обладающий высокой прочностью на сжатие, — бетону. После целлюлозы, — лигнин самый распространенный полимер на земле, играющий важную роль в природном круговороте углерода. В анализе древесины лигнин рассматривают как её негидролизуемую часть. Лигнин обеспечивает герметичность клеточных стенок (для воды и питательных веществ) и благодаря содержащимся в нем красителям определяет цвет одревесневевшей ткани. Древесина лиственных пород содержит (18-24) % (масс.доли) лигнина, хвойных — (27-30) %(масс.доли) [1].
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
В химическом смысле лигнин — понятие условное и обобщающее. Трудно найти два одинаковых лигнина. Лигнины, получаемые из разных растений, значительно отличаются друг от друга по химическому составу. Считается, что лигнин не является самостоятельным веществом, а представляет собой смесь ароматических полимеров родственного строения. Именно поэтому невозможно написать его точную структурную формулу. Принято считать, что молекула лигнина состоит из атомов водорода, кислорода и углерода. На рисунке 1 приведено представление химической структуры лигнина рекомендуемое Международным институтом лигнина. Общей структурной единицей всех видов лигнина является фенилпропан (C9H10), а различия связаны с разным содержанием функциональных групп.
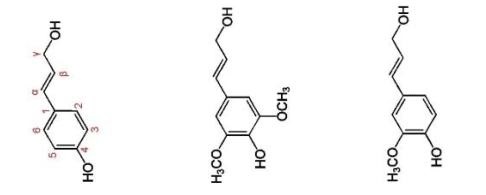
При нормальных условиях лигнин плохо растворяется в воде и органических растворителях. В химических технологиях и в окружающей среде лигнин может участвовать в самых разнообразных химических реакциях и превращениях. Обладает биологической активностью. Лигнин проявляет пластические свойства при повышенном давлении и температуре, особенно во влажном состоянии.
Основным продуктом разложения лигнина в природе является гумус. Декомпозиция лигнина в естественных условиях происходит в присутствии других элементов растительной ткани — целлюлозы и гемицеллюлозы.
Лигнин — ценное химическое сырьё, используемое во многих производствах и в медицине[2].
Пожароопасные свойства: Горючий порошок. Температура самовоспламенения: аэрогеля 300 °C, аэровзвеси 450 °C; нижний концентрационный предел распространения пламени 40 г/м³; максимальное давление взрыва 710 кПа; максимальная скорость нарастания давления 35 МПа/с; минимальная энергия зажигания 20 мДж; минимальное взрывоопасное содержание кислорода 17 %(об.доли). Тушение производят воздушно-механической пеной или распылением воды[3].
С точки зрения экономики, ежегодно в мире получается около 70 млн. тонн технических лигнинов. Условно считается, что лигнин является ценным источником химического сырья. По данным Международного института лигнина в мире используется на промышленные, сельскохозяйственные и др. цели не более 2%(масс.доли) технических лигнинов. Остальное сжигается в энергетических установках или захоранивается в могильниках.
В гидролизной промышленности получают порошковый, так называемый гидролизный лигнин.
Гидролизный лигнин представляет собой твердый остаток после отработки древесины и растительных сельскохозяйственных отходов (0,5-1,0)%-ым раствором серной или соляной кислот методом перколяции через слой при температуре (453-463)К и давлении (1,2-1,5) МПа. Это полидисперсный продукт с размером частиц от нескольких сантиметров до 1 мкм и менее. В связи с растительным происхождением гидролизный лигнин обладает значительно развитой внутренней поверхности.
По химическому составу технический гидролизный лигнин представляет собой сложный комплекс веществ различных по своей природе. В его состав входят: значительно измененный собственно лигнин растительной клетки, часть полисахаридов, не отмытые после гидролиза моносахара, минеральные и органические кислоты, зольные элементы и другие вещества. Основная доля принадлежит собственно лигнину (40 -88)%(масс.доли), трудно гидролизуемые полисахариды составляют (13 — 45)%(масс.доли), смолистые вещества и вещества лигногуминового комплекса (5 — 19)%(масс.доли), а зольные элементы (0,5 — 10)%(масс.доли)[5]. Повышенное содержание золы в техническом гидролизном лигнине объясняется плохим условием хранения сырья и его транспортировки. Это так называемая вторичная зола не характерна для древесины. Остаточное содержание кислоты в лигнине может составлять (1 -5)%(масс.доли).
Одним из перспективных и экономически выгодных направлений термической переработки гидролизного лигнина является получение на его основе углеродных адсорбентов[4].
В качестве исходного материала для получения углеродных адсорбентов гидролизный лигнин обладает рядом достоинств:
- проявляет термореактивные свойства, его термическое разложение протекает без плавления и вспучивания с образованием в твердом остатке угля;
- выход угля при термическом разложении составляет (42 — 57)%(масс.доли);
- имеет высокое содержание летучих, (60% (масс.доли) в расчете на массу горючих веществ), что позволяет в значительной степени развить пористость в угле на стадии карбонизации;
- высокая относительная подвижность макромолекул лигнина и их фрагментов облегчает его механическую переработку (измельчение, формование) и позволяет целенаправленно менять пористую структуру получаемых углей;
- карбонизованныйлигниновый уголь имеет высокую реакционную способность в процессе парогазовой активации;
- огромные запасы гидролизного лигнина и источники для его
получения гарантируют устойчивость сырьевой базы.
Трудность с использованием гидролизного лигнина связана с нестабильностью его химического состава. Соотношение основных компонентов в нем колеблется в широких пределах и зависит от вида растительного сырья и режима гидролиза. В таблице 1 представлен средний состав гидролизного лигнина.
Таблица 1 — Характеристика гидролизного лигнина
| Наименование компонентов | Содержание, % в пересчете на абсолютно сухие Вещества | |
| Лигнин из древесины | Лигнин из сельскохозяйственных отходов | |
| Влажность | 58-80 | 58-80 |
| Зольность | 0,7 — 9,6 | 0,5 — 10,9 |
| Кислотность (в пересчете на H2SO4) | 0,4 — 2,4 | 0,6-1,3 |
| Редуцирующие вещества | 1,1-10,0 | 0,1-9,6 |
| Вещества экстрагируемые спирт -бензольной смесью | 7,6-19,1 | 5,4-8,3 |
| Полисахариды | 12,6-31,9 | 3,1-45,2 |
| Собственно лигнин | 48,3 — 72,0 | 38,9-87,5 |
1.6.2. Хвоя, как перспективный сорбент на основе растительного сырья
Одной из современных приоритетных задач в области защиты окружающей среды является поиск эффективных и экологически безопасных технологий очистки сточных вод. Перспективным направлением является технология, основанная на использовании сорбентов.
При выборе сорбционных материалов следует руководствоваться такими параметрами как величина сорбции, стоимость, доступность, эффективность, возможность применения вторичных материальных ресурсов, экологическая безопасность утилизации насыщенных сорбентов.
В соответствии с перечисленными критериями выполнен анализ эффективности применяемых сорбентов. Сорбенты на основе неорганических материалов обладают невысокой сорбционной емкостью, гидрофильны, требуют дополнительного модифицирования, вызывают трудности с утилизацией. Синтетические сорбенты удобны благодаря хорошей поглотительной способности, доступности, однако отличаются большой стоимостью, сложностью переработки в силу высокой токсичности продуктов горения. Наиболее привлекательны сорбенты из отходов растительного сырья. Практически неограниченные запасы этих материалов, их дешевизна, простая технология получения, экологическая безопасность процессов переработки использованных сорбентов, а также довольно высокие адсорбционные, ионообменные и фильтрационные свойства сорбентов стимулируют исследования, направленные на получение новых адсорбционно-активных материалов из растительного сырья.
Одним из видов растительного сырья является хвоя.
Хвоя является листоподобным органом многих голосеменных (хвойных) растений — сосны, ели, туи и др. Ювенильная хвоя чаще всего бывает игловидной, заостренной, иногда серповидно изогнутой. Зрелая хвоя многих растений становится чешуевидной, укороченной. Хвоя содержит ценные биологические компоненты: хлорофилл (до 1,4 %(масс.доли)), витамины, макро- и микроэлементы, фитогормоны, фитонциды, бактериостатические и антигельминтные вещества.
В еловой хвое содержатся многие аминокислоты, в том числе и незаменимые.
Хвоя большинства растений (ель, сосна, пихта, можжевельник, кипарис и др.) используется в фармакологии, ароматерапии и парфюмерии. Из хвои сосны и ели получают витаминные препараты.
Сосновая хвоя обладает уникальными свойствами. Она экологичная, натуральная, наделена увеличенными целебными свойствами. Ее можно использовать:
- как кормовую добавку в животноводстве;
- для создания хвойно-витаминной муки;
- изготовления экстрактов для принятия хвойных ванн;
- для изготовления эфирного масла;
- для производства хвойного воска;
- как сорбент растительного происхождения.
Сосновые иголки – то, что можно встретить в каждом хвойном бору. Заводов по переработке сосновой хвои мало, а это значит, что ежегодно тонны природного материала остаются невостребованными. Вместе с тем хвоя, которую топчут под ногами лесники, грибники, может принести значительный доход, который может выражаться в миллионах рублей.
Глава 2. Цель и задачи работы
Цель работы – получить сульфокатиониты путем сульфирования гранулированных ионообменных материалов из смеси лигнина и хвои, полученных фосфорнокислотной активацией.
Задачи:
1. Отработать технологию получения сульфокатионитов путем сульфирования гранулированных ионообменных материалов из смеси лигнина и хвои, полученных фосфорнокислотной активацией.
1.1. Оптимизировать технологические параметры получения гранулированных ионообменных материалов из смеси лигнина и хвои методомфосфорнокислотной активации.
1.2. Исследовать влияние стадии сульфирования на эксплуатационные характеристики сульфокатионитов.
2. Исследовать пористую структуру и основные сорбционные и ионообменные характеристики полученных сульфокатионитов.
3. Исследовать кинетику поглощения катионов меди из водных растворов.
4. Изучить работу сульфокатионитов в цикле.
5. Определить химию поверхности полученных сульфокатионитов.
Глава 3. Экспериментальная часть
3.1. Технология получения фосфорнокислых катионитов из смеси лигнина и хвои с добавлением фосфорной кислоты
3.1.1. Исходное сырье
В качестве исходного сырья использовались хвоя, гидролизный лигнин и 40% фосфорная кислота.
3.1.2. Помол хвои
Сухие хвойные иголки измельчались в кофемолке и просеивались через сито с диаметром отверстий 0,1 см.
3.1.3. Подсушка лигнина
Гидролизный лигнин сушился при температуре (100-110) 0С до остаточной влажности 0% (масс.доли) и измельчался в кофемолке до порошкообразного состояния.
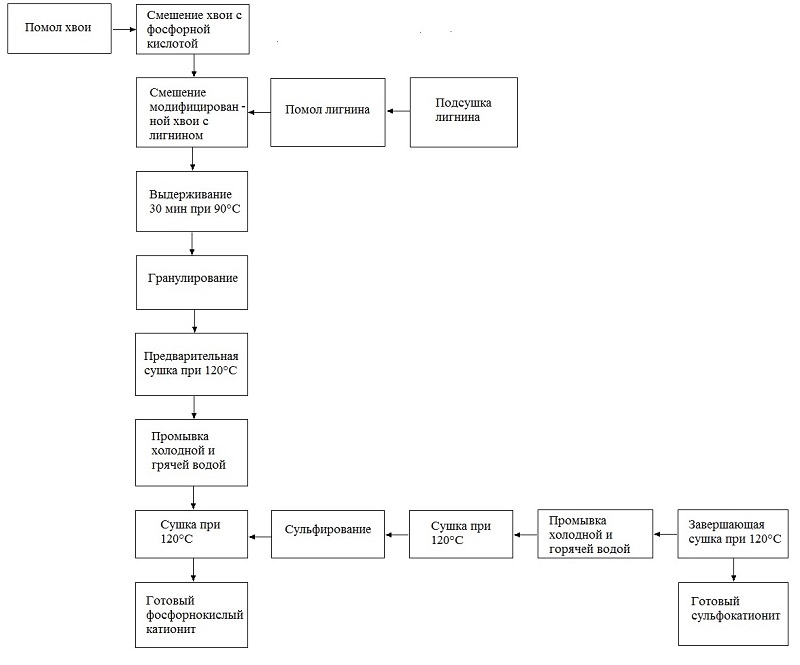
3.1.4. Смешение лигнина и хвои с фосфорной кислотой. Гранулирование
Пропитку исходного сырья проводили фосфорной кислотой. Смешение полученного материала производили в ручную в стеклянном кристаллизаторе при постоянном перемешивании в течение 60 мин с подогревом при температуре 90°С до однородного состояния. Соотношение смеси к сульфирующему агенту – 1:1,5 по массе. Фосфорная кислота при контакте с сырьем одновременно является водоотнимающим и фосфирующимагентом.
Гранулирование происходит на гидравлическомгрануляторе.
3.1.5. Сушка
После гранулирования образцы отправляются на предварительную сушку в течение 24 ч при 120°C.
3.1.6. Промывка
Определено, что промывка водой полуфабриката должна обеспечивать не только удаление отработанной фосфорной кислоты, но и растворимых в нейтральных и щелочных растворах полупродуктов разложения.
Промывка порошкового катионита осуществлялась на водоструйном насосе, гранулированный ионит отмывался декантацией. Для отмывки на первых стадиях использовалась дистиллированная вода, в дальнейшем – водопроводная.
3.1.7. Сушка
Сушку сульфокатионита от влажности (65±5)%(масс.доли) до (35±5)%(масс.доли) можно проводить в течение 15 ч в естественных условиях или в сушилке при температуре (120±5)°С в течение 120 мин.
3.1.8. Сульфирование
Некоторые образцы уже готового фосфорнокислого катионита подвергались сульфированию,т.е. в них были введены сульфогруппы (-SO3H) обработкой 20-ти и 40%-ой серной кислотой в течение 48 ч. Далее образцы сушились в течение 120 мин, повторно отмывались и проходили завершающую сушку при температуре (120±5)°С в течение суток.
Глава 4. Методика исследования катионитов
4.1. Определение полной статической обменной емкости Н-катионита по 0,1 н. раствору едкого натра
Сущность метода.
Полная обменная емкость катионита определяются количеством всех активных ионогенных групп, входящих в его состав, в условиях, обеспечивающих их полную ионизацию, и является постоянной величиной, соответствующей состоянию предельного насыщения всех способных к ионному обмену активных групп данного катионита. Метод заключается в титровании навески катионита в Н-форме раствором щелочи, с последующим обратным титрованием ее избыточного количества раствором соляной кислоты[19].
Методика определения.
Навеску Н-катионита в количестве, приблизительно соответствующем 1 г сухого продукта, взвешенную на аналитических весах с точностью до 0,001 г, помещают в плоскодонную коническую колбу вместимостью 0,25 дм3, куда прибавляют 200 см3 0,1 н. раствора едкого натра. Колбу закрывают пробкой и оставляют при комнатной температуре на (24-48) ч, периодически перемешивая катионит с раствором. На стенках колбы не должно находиться частиц катионита. После (24-48) ч (или более длительного) контакта, не прореагировавший раствор отфильтровывают в сухую колбу, 25 см3 фильтрата титруют 0,1 н. раствором соляной кислоты в присутствии 2 — 3 капель смешанного индикатора до достижения устойчивой окраски раствора.
Расчет обменной емкости проводили по формуле:
Eполн = [(200k1N1 – 8ak2N2)*100]/[m*(100-W)], (1)
где Еполн— полная статическая обменная емкость катионита по 0,1 н. раствору NaОН, мг-экв/г;
а – количество 0,1 н. раствора HCl, пошедшего на титрование, см3;
к1 – поправочный коэффициент 0,1 н. раствора NaOH;
к2 – поправочный коэффициент 0,1 н. раствора HCl;
N1 – теоретическая нормальность раствора NaOH;
N2 – теоретическая нормальность раствора HCl;
m– навеска ионита, г;
W — влажность катионита, %(масс.доли).
4.2. Определение равновесной обменной емкости Н-катионита по 0,1 н. раствору хлорида натрия
Сущность метода заключается в титровании раствором щелочи кислоты, выделившейся в результате ионного обмена Н-формы катионита с раствором электролита – хлорида натрия в равновесных условиях опыта [19].
Методика определения. Навеску Н-катионита в количестве, приблизительно соответствующем 1г сухого продукта, взвешенную на аналитических весах с точностью до 0,001 г, помещают в плоскодонную коническую колбу вместимостью 0,25 дм3, куда прибавляют 200 см3 0,1 н. раствора NaCl. Колбу закрывают пробкой и оставляют при комнатной температуре на (24-48) ч, периодически перемешивая катионит с раствором. На стенках колбы не должно находится частиц катионита. После (24-48) ч (или более длительного) контакта, непрореагировавший раствор отфильтровывают в сухую колбу, 25 см 3 фильтрата титруют 0,1 н. раствором едкого натра в присутствии 2-3 капель метилового оранжевого до достижения устойчивой окраски раствора.
Расчет обменной емкости производят по формуле:
Eполн = [8ak2N2*100]/[m*(100-W)], (2)
гдеEполн — равновесная статическая обменная емкость катионита по 0,1н. раствору NaCl, мг-экв/г;
а – количество 0,1 н. раствора NaOH, пошедшего на титрование,см3;
к – поправочный коэффициент 0,1 н. раствора NaOH;
N – теоретическая нормальность раствора едкого натра;
m– навеска ионита, г;
W — влажность катионита, % (масс.доли).
4.3. Определение равновесной обменной емкости Н-катионита по 0,1 н. раствору хлорида кальция
Сущность метода заключается в титровании раствором щелочи кислоты, выделившейся в результате ионного обмена Н-формы катионита с раствором электролита – хлорида натрия в равновесных условиях опыта.
Методика определения.
Навеску Н-катионита в количестве, приблизительно соответствующую 1г сухого продукта, взвешенную на аналитических весах с точностью до 0,001 г, помещают в плоскодонную коническую колбу вместимостью 0,25 дм3, куда прибавляют 100 см3 0,1 н. раствора CaCl2 . Колбу закрывают пробкой и оставляют при комнатной температуре на (24-48) ч, периодически перемешивая катионит с раствором. На стенках колбы не должно находиться частиц катионита. После (24-48) ч (или более длительного) контакта, непрореагировавший раствор отфильтровывают в сухую колбу, 25 см3 фильтрата титруют 0,1 н. раствором едкого натра в присутствии (2-3) капель смешанного индикатора до достижения устойчивой окраски раствора [19].
Расчет обменной емкости производят по формуле:
Eполн = [4ak2N2*100]/[m*(100-W)], (3)
где Eполн— равновесная статическая обменная емкость катионита по 0,1 н.раствору СaCl2, мг-экв/г;
а – количество 0,1 н. раствора NaOH, пошедшего на титрование,см3;
к – поправочный коэффициент 0,1 н. раствора NaOH;
N – теоретическая нормальность раствора едкого натра;
m– навеска ионита, г;
W — влажность катионита, % (масс.доли).
4.4. Определение сорбционной активности по ионам меди 2+
Навеску 1г помещаем в колбу с раствором сульфата меди с концентрацией 5%(масс.доли)и 0,05% (масс. доли) и выдерживаем 15, 30, 60, 120 мин. Отбираем 1 см3 раствора меди из колбы и разбавляем 40 см3 дистиллированной воды. Прибавляем 2 см3 10%-ного раствора роданистого калия (KCNS) и 2 см3 10%-ного раствора йодистого калия (KJ). Титруем тиосульфатом натрия (Na2S2O3).
Сорбционную активность (в мг-экв/г) вычисляем по формуле:
X = [(V1-V2)*0.006357*500]/[1*my], (4)
где V1 – объем 0,1 н. раствора тиосульфата пошедшего на титрование 1см3 исходного раствора;
V2 — объем 0,1 н. раствора тиосульфата пошедшего на титрование 1 см3 раствора с сульфокатионитом;
my – масса навески, г;
0,006357 — количество меди соответствующее 1см3 0,1 раствора тиосульфата натрия.
Глава 5. Исследование ионообменных свойств катионитов
Катиониты из бинарной смеси отходов деревообрабатывающей промышленности с добавлением в качестве химического модификатора фосфорной и серной кислоты, получали по технологии, описанной в пункте 3. В процессе определения основных характеристик полной и статических обменных емкостей (ПОЕ, СОЕ) было выявлено, что КФ и СК из смеси хвои и гидролизного лигнина превосходит промышленный сульфоуголь. Также была исследована работа различных катионитов в цикле.
Цикличная работа показала снижение ионообменной способности как на втором, так и на третьем цикле.
Небольшое повышение полной обменной ёмкости исходного гранулированного образца на третьем цикле обусловлено нестойкостью гранул в щелочной среде. Гранулы разваливаются и образуют порошок, который обладает более высокими ионообменными свойствами.
Полученные экспериментальные данные представлены в таблице 2.
Были проведены исследования по определению поглотительной способности полученных катионитов по катионам меди из водных растворов. Для этого готовился 5%-ный и 0,05%-ный водный раствор сульфата меди, в который помещалась навеска катионита массой примерно 1 грамм. Результаты исследования кинетики поглощения ионов медикатионитами представлены в таблице 3,4 и на рисунке 2.
Таблица 2 — Обменные емкости полученных катионитов
| Сорбент | Цикл | Полная обменная емкость по NaОН, мг-экв/г | Статическая обменная емкость по NaCl, мг-экв/г | Статическая обменная емкость по СaCl2, мг-экв/г |
| Катионит из хвои и гидролизного лигнина (30:70) | 1 | 8,8 | 0,8 | 0,58 |
| 2 | 8,0 | 0,75 | 0,5 | |
| 3 | 7,9 | 0,7 | 0,4 | |
| Катионит из хвои и гидролизного лигнина (30:70)+20% H2SO4 | 1 | 11,6 | 1,3 | 0,81 |
| 2 | 11,2 | 1,0 | 0,8 | |
| 3 | 11,0 | 0,8 | 0,75 | |
| Катионит из хвои и гидролизного лигнина (30:70)+40% H2SO4 | 1 | 11,0 | 1,0 | 0,7 |
| 2 | 10,5 | 0,9 | 0,6 | |
| 3 | 10,4 | 0,6 | 0,6 | |
| Катионит из хвои и гидролизного лигнина (50:50) | 1 | 9,6 | 1,0 | 0,68 |
| 2 | 9,0 | 1,0 | 0,5 | |
| 3 | 8,8 | 0,7 | 0,5 | |
| Катионит из хвои и гидролизного лигнина (50:50)+20% H2SO4 | 1 | 11,8 | 1,5 | 0,71 |
| 2 | 11,6 | 1,3 | 0,7 | |
| 3 | 11,0 | 1,2 | 0,55 | |
| Катионит из хвои и гидролизного лигнина (50:50)+40% H2SO4 | 1 | 11,0 | 1,7 | 0,74 |
| 2 | 10,2 | 1,5 | 0,6 | |
| 3 | 10,3 | 1,0 | 0,58 | |
| Катионит из хвои и гидролизного лигнина (70:30) | 1 | 10,12 | 1,0 | 0,76 |
| 2 | 9,86 | 1,0 | 0,68 | |
| 3 | 9,0 | 0,5 | 0,66 | |
| Катионит из хвои и гидролизного лигнина (70:30)+20% H2SO4 | 1 | 12,36 | 1,6 | 0,8 |
| 2 | 12,1 | 1,6 | 0,7 | |
| 3 | 11,6 | 1,55 | 0,6 | |
| Катионит из хвои и гидролизного лигнина (70:30)+40% H2SO4 | 1 | 12,28 | 1,7 | 0,82 |
| 2 | 12,0 | 1,6 | 0,8 | |
| 3 | 12,1 | 1,6 | 0,65 | |
| Промышленный сульфоуголь | 1 | 6,5 | 2,3 | 0,4 |
| 2 | 6,28 | 0,43 | 0,61 |
Результаты исследования кинетики поглощения ионов медикатионитами представлены ниже.
Таблица 3 — Результаты исследования кинетики поглощения ионов меди из 5%(масс.доли) раствора
| Сорбент | Поглотительная способность, мг-экв/г | ||||
| 20 минут | 40 минут | 60 минут | 120 минут | Сутки | |
| Катионит из хвои и гидролизного лигнина (30:70) | 0,95 | 1,27 | 1,59 | 2,22 | 2,54 |
| Катионит из хвои и гидролизного лигнина (30:70)+20% H2SO4 | 0,64 | 1,27 | 1,59 | 1,91 | 2,22 |
| Катионит из хвои и гидролизного лигнина (30:70)+40% H2SO4 | 0,95 | 1,59 | 1,59 | 1,91 | 2,22 |
| Катионит из хвои и гидролизного лигнина (50:50) | 1,27 | 1,59 | 1,91 | 2,22 | 2,54 |
| Катионит из хвои и гидролизного лигнина (50:50)+20% H2SO4 | 0,95 | 1,27 | 1,91 | 2,22 | 2,22 |
| Катионит из хвои и гидролизного лигнина (50:50)+40% H2SO4 | 0,95 | 1,27 | 1,59 | 1,91 | 2,22 |
| Катионит из хвои и гидролизного лигнина (70:30) | 1,27 | 1,59 | 1,91 | 2,54 | 2,86 |
| Катионит из хвои и гидролизного лигнина (70:30)+20% H2SO4 | 1,27 | 1,59 | 1,91 | 2,54 | 2,86 |
| Катионит из хвои и гидролизного лигнина (70:30)+40% H2SO4 | 0,95 | 1,27 | 1,59 | 1,91 | 2,54 |
| Промышленный сульфоуголь | 0,25 | 0,35 | 0,49 | 0,53 | 0,64 |
Таблица 4 — Результаты исследования кинетики поглощения ионов меди из 0,05%(масс.доли) раствора
| Сорбент | Поглотительная способность, мг-экв/г | ||||
| 20 минут | 40 минут | 60 минут | 120 минут | Сутки | |
| Катионит из хвои и гидролизного лигнина (30:70) | 0,32 | 0,64 | 0,95 | 0,95 | 1,27 |
| Катионит из хвои и гидролизного лигнина (30:70)+20% H2SO4 | 0,32 | 0,32 | 0,64 | 0,95 | 0,95 |
| Катионит из хвои и гидролизного лигнина (30:70)+40% H2SO4 | 0,32 | 0,32 | 0,32 | 0,64 | 0,64 |
| Катионит из хвои и гидролизного лигнина (50:50) | 0,32 | 0,32 | 0,95 | 0,95 | 1,27 |
| Катионит из хвои и гидролизного лигнина (50:50)+20% H2SO4 | 0,32 | 0,64 | 0,95 | 0,95 | 1,27 |
| Катионит из хвои и гидролизного лигнина (50:50)+40% H2SO4 | 0,32 | 0,95 | 0,95 | 0,95 | 0,95 |
| Катионит из хвои и гидролизного лигнина (70:30) | 0,32 | 0,32 | 0,64 | 0,95 | 1,27 |
| Катионит из хвои и гидролизного лигнина (70:30)+20% H2SO4 | 0,32 | 0,32 | 0,64 | 0,95 | 0,95 |
| Катионит из хвои и гидролизного лигнина (70:30)+40% H2SO4 | 0,32 | 0,32 | 0,64 | 0,95 | 0,95 |
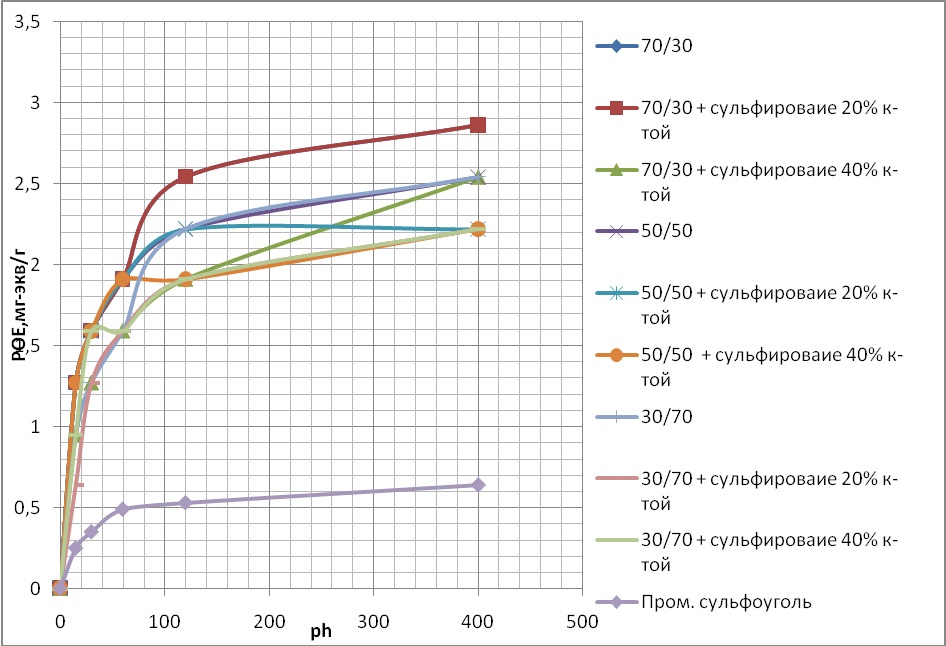
Исследование кинетики поглощения катионов меди из водных растворов данными СК показали, что почти все предложенные образцы обладают лучше кинетикой, чем промышленный сульфоуголь.
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
