или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Содержание
- Введение
- Глава 1. Аналитический обзор
- 1.1. Очистка ионным обменом
- 1.2. Основы синтеза ионообменных смол
- 1.3. Сульфокатиониты. Получение и свойства
- 1.4. Альтернативные способы получения сульфокатионитов
- 1.5. Фосфорнокислые катиониты
- 1.6. Характеристики сырья
- Глава 2. Цель и задачи работы
- Глава 3. Экспериментальная часть
- 3.1. Технология получения фосфорнокислых катионитов из смеси лигнина и хвои с добавлением фосфорной кислоты
- Глава 4. Методика исследования катионитов
- 4.1. Определение полной статической обменной емкости Н-катионита по 0,1 н. раствору едкого натра
- 4.2. Определение равновесной обменной емкости Н-катионита по 0,1 н. раствору хлорида натрия
- 4.3. Определение равновесной обменной емкости Н-катионита по 0,1 н. раствору хлорида кальция
- 4.4. Определение сорбционной активности по ионам меди 2+
- Глава 5. Исследование ионообменных свойств катионитов
- Глава 6. Определение зависимости обменной емкости катионита от рН-раствора с помощью кривых потенциометрического титрования
- Глава 7. Методика определения поверхностных функциональных групп
- Глава 8. Исследование пористой структуры
- 8.1. Определение адсорбционной активности по метиленовому голубому
- 8.2. Методика определения предельного объёма сорбционного пространства
- Глава 9. Эксплуатационные и прочностные характеристики
- Список использованных источников
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
Введение
В связи с экологической напряженностью проблема получения и поиска новых сорбентов, так же как и разработка новых сорбционных технологий, является актуальной. Особый интерес представляют многотоннажные производства, такие как, например, лесоперерабатывающая и лесохимическая промышленности. Последнее объясняется двумя причинами. С одной стороны, технологии этих производств обременены значительными отходами. С другой – древесина и ее компоненты, природные соединения являются сырьем для получения сорбентов.
Одним из потенциальных направлений использования углеродсодержащих отходов являются гидролизные лигнины растительного происхождения и отходы деревообрабатывающей промышленности (опилки, хвоя).
Как продукт фосфорнокислотногообугливания различных видов органического сырья, в том числе гидролизного лигнина и хвои можно получить фосфорнокислые катиониты(КФ). В настоящее время этот процесс малоизучен. Однако развитие данного направления позволило бы уменьшить экологическую нагрузку на окружающую среду и получить полезные продукты для природооханных целей с небольшими затратами энергии и реагентов.
Одним из направлений использования таких сорбентов являются ионообменные процессы для обессоливания воды и очистки сточных вод от ионов металлов, а также сорбция радионуклидов.
Таким образом, разработка эффективного способа получения катионитов из древесных отходов на современном этапе является актуальной задачей.
Глава 1. Аналитический обзор
1.1. Очистка ионным обменом
В настоящее время ионообменные процессы широко используются для обессоливания воды и очистки сточных вод от ионов металлов. Ионным обменом называется процесс обмена ионов твердой матрицы ( ионита ) с ионами воды. Это химический процесс, имеющий некоторое сходство с адсорбцией (поглощением), физическим процессом. При ионном обмене, как и при адсорбции, реакции протекают в двух фазах, например, в твердой и жидкой. Характерным отличием между этими процессами является то, что ионный обмен представляет собой химическую реакцию взаимного обмена между ионами ионообменного материала и раствора. Ионный обмен сопровождается выделение в раствор эквивалентного количества ионов того же знака заряда, которые были сорбированы из раствора.
Наличие разнообразных ионообменных материалов позволяет решать задачи очистки вод различного химического состава с высокой эффективностью. Это единственный метод, дающий возможность выборочно, селективно извлекать из раствора некоторые компоненты, например, соли жесткости, тяжелые металлы.
В процессах, в которых участвуют ионообменные материалы, особенно ионообменные смолы, наряду с ионным обменом и адсорбцией могут протекать окислительно – восстановительные реакции и реакции образования слабодиссоциированных соединений.
Ионообменные материалы (иониты) – естественные и искусственные, неорганические и органические, твердые и жидкие, практически нерастворимые в воде и других растворителях полиэлектролиты, имеющие в структуре специальные функциональные ионоогенные группы, способные к реакциям обмена ионов с ионами раствора(электролитами). Этим понятием объединяются все иониты, независимо от их природы.
Ионообменные смолы – искусственные высокомолеулярные органические, практически нерастворимые в воде и других растворителях полиэлектролиты, обладающие ионообменными свойствами.
При ионизации функциональных групп возникают две разновидности ионов: одни жестко закреплены на каркасе (матрице) R ионита, другие – противоположного им знака (противоионы), способные переходить в раствор в обмен на эквивалентное количество других ионов того же знака из раствора[6].
Основной характерной чертой ионообменных материалов является наличие у них ионогенных групп. По характеру этих групп все ионообменные материалы разделяются на катиониты (полимерные кислоты), содержащие кислотные группы, и аниониты (полимерные основания), содержащие основные группы. Помимо этих двух групп, существуют амфолиты (амфотерные полиэлектролиты), обладающие свойствами катионитов и анионитов одновременно.
Катионитами называются иониты с закрепленными на матрице анионами или анионообменными группами, обменивающиеся с внешней средой катионами.
Если катионит находился в водородной Н+ — форме то извлекаются все катионы, находящиеся в воде. Очищенный раствор имеет кислую реакцию.
При движении через катионит раствора, содержащего смесь катионов, таких как Na, Ca, Mg, Fe (природная вода), происходит формирование в его слое фронтов сорбции каждого катиона и неодновременное начало проскока их в фильтрат. Очистку заканчивают при появлении в фильтрате основного извлекаемого или контролируемого иона[7].
Аниониты – иониты с закрепленными на матрице катионами или катионообменными группами, обменивающиеся с внешней средой анионами. Если анионит находится в гидроксильной ОH – — форме, то на очистку от анионов подается, как правило, раствор после контактирования с катионитом в Н+ — форме, имеющий кислую реакцию. В этом случае извлекаются все находящиеся в растворе анионы. Очищенный раствор имеет нейтральную реакцию[16].
При пропускании через анионит раствора, содержащего смесь анионов, таких как Cl, SO4 , PO4 , NO3 , происходит формирование в его слое фронтов сорбции каждого иона и неодновременное начало проскока их в фильтрат. Очистка воды заканчивается при появлении в фильтрате извлекаемого иона.
Амфолиты содержат закрепленные катионообменные и анионообменные группы, и в определенных условиях выступают либо как катионит, либо как анионит. Используются для переработки технологических растворов. Являясь высокомолекулярными кислотами и основаниями, иониты в зависимости от степени диссоциации, а, следовательно, и от подвижности способных к обмену ионов, могут быть разделены на четыре типа:
- иониты (катиониты и аниониты), проявляющие свойства сильных кислот и оснований, сильнокислотные катиониты и сильноосновные аниониты; рК<2;
- иониты (катиониты и аниониты), проявляющие свойства слабых кислот и оснований, — слабокислотные катиониты и слабоосновные аниониты; рК≥4;
- иониты смешанного типа, проявляющие свойства одновременно смеси сильной и слабой кислот или сильного и слабого основания;
- иониты, обменная емкость которых непрерывно возрастает по мере повышении рН (для катионитов) и рОН(для анионитов) в широком интервале значений.
По структуре матрицы ионообменные смолы делятся на:
- гелевые — микропоры имеют молекулярные размеры. Они представляют собой гомогенные поперечносвязанные полимеры. Фиксированные ионы равномерно распределены по всему объему полимера. Гелевые ионообменные смолы обладают высокой обменной емкостью, однако характеризуются невысокой скоростью обмена;
- макропористые — размеры пор смолы имеют размеры в десятки нанометров. Имеют фиксированную систему пор и каналов, определяемую условиями синтеза. Обменная ёмкость таких смол меньше, чем гелевых при высокой скорости обмена.
В последние годы при глубоком изучении химических свойств ионитов было обнаружено, что многие из них обладают окислительно – восстановительными (КУ-1, АН-2Ф) и комплексообразовательными свойствами (аниониты на основе полиэтилен-полиамина: ЭДЭ-10П, АВ-16, АН-31). Указанные свойства зависят как от химического строения полимера (АН-2Ф, ЭДЭ-10П), так и от наличия в нем растворимых примесей и фракций; так, например, полимеры АВ-17 и АВ-18 обладают окислительно – восстановительными и комплексообразовательными свойствами благодаря присутствию в них различных примесей.
В настоящее время синтезированы полимеры, обладающие только ионообменными, окислительно – восстановительными, комплексообразующими или же смешанными свойствами. Но, несмотря на это, пока все реакционноспособные синтетические полимеры называются ионитами, ионообменными смолами, сорбентами, электрообменниками, селективными ионитами и т.д.
Основными характеристиками ионитов являются:
- обменная емкость;
- селективность;
- механическая прочность;
- химическая стабильность;
- температурная устойчивость[17].
Для количественной характеристики ионообменных и сорбционных свойств ионитов применяют следующие величины: полная, динамическая и рабочая обменная емкость.
Полная обменная емкость ( ПОЕ ) определяется числом функциональных групп, способных к ионному обмену, в единице массы воздушно-сухого или набухшего ионита и выражается в мг-экв/г или мг-экв/л. Она является постоянной величиной, которую указывают в паспорте ионита, и не зависит от концентрации или природы обменивающегося иона. ПОЕ может изменяться (уменьшаться) из-за термического, химического или радиационного воздействия. В реальных условиях эксплуатации ПОЕ уменьшается со временем вследствие старения матрицы ионита, необратимого поглощения ионов-отравителей (органики, железа и т. п.), которые блокируют функциональные группы.
Равновесная (статическая) обменная емкость зависит от концентрацииионов в воде, рН и отношения объемов ионита и раствора при измерениях. Необходима для проведения расчетов технологических процессов.
Динамическая обменная емкость (ДОЕ) важнейший показатель в процессах водоподготовки. В реальных условиях многократного применения ионита в цикле сорбции-регенерации обменная емкость используется не полностью, а лишь частично. Степень использования определяется методом регенерации и расходом регенерирующего агента, временем контакта ионита с водой и с регенерирующим агентом, концентрацией солей, рН, конструкцией и гидродинамикой используемого аппарата.
Селективность. Под селективностью понимают способность избирательно сорбировать ионы из растворов сложного состава. Селективность определяется типом ионогенных групп, числом поперечных связей матрицы ионита, размером пор и составом раствора. Для большинства ионитов селективность невелика, однако разработаны специальные образцы, имеющие высокую способность к извлечению определенных ионов.
Механическая прочность показывает способность ионита противостоять механическим воздействиям. Иониты проверяются на истираемость в специальных мельницах или по весу груза, разрушающего определенное число частиц. Все полимеризационные иониты имеют высокую прочность. У поликонденсационных она существенно ниже. Увеличение степени сшивки полимера повышает его прочность, но ухудшает скорость ионного обмена.
Химическая стабильность. Все иониты обладают определенной стойкостью к растворам кислот, щелочей и окислителей. Все полимеризационные иониты имеют большую химическую стойкость, чем поликонденсационные. Катиониты более стойки, чем аниониты. Среди анионитов слабоосновные устойчивее к действию кислот, щелочей и окислителей, чем сильноосновные.
Температурная устойчивость катионитов выше, чем анионитов. Слабокислотные катиониты работоспособны при температуре до 130 °С, сильнокислотные типа КУ-2-8 – до (100–120) °С, а большинство анионитов – не выше 60°С, максимум 80 ° С. При этом, как правило, Н- или
ОН-формы ионитов менее стойки, чем солевые.
Ионообменные сорбенты, в частности катиониты, играют важную роль в различных сферах хозяйственной деятельности [8].
В основном они применяются:
- для умягчения и обессоливания воды в теплоэнергетике и других отраслях;
- для разделения и выделения цветных и редких металлов в гидрометаллургии;
- при очистке возвратных и сточных вод;
- для регенерации отходов гальванотехники и металлообработки;
- для разделения и очистки различных веществ в химической промышленности;
- в качестве катализатора для органического синтеза.
Катиониты используются в котельных, теплоэлектростанциях, атомных станциях, пищевой промышленности (при производстве сахара, алкогольных, слабоалкогольных и других напитков, пива, бутилированной воды), фармацевтической промышленности и других отраслях.
1.2. Основы синтеза ионообменных смол
В основе синтеза ионообменных смол лежат реакции, которые применяют в синтезе высокомолекулярных соединений, т.е. реакции полимеризации и поликонденсации.
В настоящее время в промышленных масштабах освоено производство многих образцов ионообменных смол, синтезированных из различных веществ и, кроме того, различающихся методами их синтеза и характером ионогенных групп. Неисчерпаемые возможности современного органического синтеза позволяют создавать ионообменные смолы с самыми разнообразными свойствами.
Наиболее важные свойства ионообменных смол в значительной степени определяются химической природой и структурой макромолекулярного каркаса смолы. Так, например, для эффективности ионного обмена очень важное значение имеет проницаемость зерен ионита по отношению к сорбируемым ионам, а для проницаемости зерен ионита – степень его набухаемости, которая в свою очередь зависит от химической природы с структуры макромолекулярного каркаса смолы, главным образом от размера ячейки макромолекулярной решетки. Так, чем больше размер ячейки, тем более проницаема смола для крупных ионов. Но слишком большие размеры ячеек приводят к понижению механических свойств ионообменника. Сырьем для получения органических ионообменных смол служат органические вещества, так называемые мономеры, которые способны в результате реакции полимеризации или поликонденсации образовывать высокомолекулярные соединения. Ионогенные группы могут содержаться в мономерах или вводиться в уже готовые полимеры (полимераналогичные превращения).
В связи с этим существуют два метода синтеза ионитов:
- Полимеризация или поликонденсация мономеров, содержащих в своих молекулах ионогенные группы.
- Синтез полимера, затем его химическая обработка с целью введения ионогенных групп.
В зависимости от способа образования макромолекулы полимера иониты бывают поликонденсационного или полимеризационного типа.
Для создания трехмерного макромолекулярного каркаса поликонденсационных ионитов используют органические вещества, содержащие в молекуле не менее трех реакционноспособных групп или атомов, т.е. трехфункциональные мономеры (фенол, анилин, меламин и т. д.), которые при реакции конденсации, например, с формальдегидом, дают неплавкие, нерастворимые полимеры, содержащие ионогенные группы.
При получении ионообменных смол полимеризационного типа обычно используют виниловые или другие двухфункциональные мономеры, но в этом случае для сшивки линейных полимеров, т. е. для создания межцепных поперечных связей их сополимеризуют с дивинильными мономерами – кроссагентами (дивинилбензолом, диметакриловым эфиром этиленгликоля и т. д.).
При синтезе полимера можно регулировать размеры ячеек макромолекулярного каркаса путем подбора подходящего кроссагента, а также изменения количественного соотношения между кроссагентом и мономером, служащим для построения линейной цепи полимера.
В последнее время развилось новое направление в создании ионитов с различной проницаемостью. При синтезе удается не только регулировать размеры ячеек, но и создавать «поры» внутри полимера путем обрыва линий его цепи. Обрыв достигается телогенированием, т.е. получением в линейных цепях не полимера, а теломера – короткой цепи. В качестве телогена – вещества, тормозящего рост линейной цепи, используют чаще всего четыреххлористый углерод. Его вводят при получении сополимера в количестве около 10% (масс.доли).
Полученные таким образом иониты носят название телогенированных, или микропористых.
Процессы полимеризации или поликонденсации при получении ионитов можно проводить блочным или суспензионным способом. В первом случае при дроблении блоков получают зерна смолы неправильной формы. При суспензионной полимеризации или поликонденсации получают гранулы правильной сферической формы. Последние имеют большую механическую прочность. Одно из преимуществ синтетических органических ионитов (ионообменных смол) состоит в том, что им можно придать любую технологическую форму – стержней, пластин, цилиндров, волокон, тканей, сосудов и т.д.
Важным моментом в развитии технологии ионитов является получение макропористых ионитов. Макропористые иониты получают введением в реакционную массу в процессе полимеризации (или поликонденсации) инертного растворителя, например изооктана, который захватывается массой, а затем уже удаляется из пространственного полимера. Ионит представляет собой как бы затвердевшую губку. Макропористые иониты имеют повышенные механические, а так же кинетические характеристики по сравнению с обычными ионитами, так как поры облегчают диффузию ионов к активным центрам.
Широкое распространение ионитов сдерживается относительно высокой стоимостью этих сорбентов, которая объясняется многостадийностью процессов их получения. Эти трудности производства связаны с высокой стоимостью древесного сырья и модификаторов. Помимо экономических факторов определённые ограничения развития производства катионообменных материалов связаны и с тем, что при их получении в промышленном масштабе в качестве исходных соединений используются токсичные вещества, такие как бензол, фенолы и другие, а источником ионообменных сорбентов является невозобновляемое органическое сырье. Расширение объемов и необходимость утилизации отходов деревопереработки, а также разработка способов извлечения и повторного многократного использования модификатора в производстве существенно повысили стабильность и стоимостные показатели получаемых углеродных адсорбентов. Таким образом, большой интерес представляет создание ионообменных сорбционных материалов из возобновляемого растительного сырья, в частности из древесины.
Производство сорбентов из отходов древесины началось еще с 30-х годов 20-го века. К преимуществам этого способа получения углеродных сорбентов относится:
- высокие адсорбционные и механические характеристики получаемых сорбентов;
- отходы древесины являются наиболее доступным сырьем, постоянно возобновляющимся в процессах фотосинтеза.
Недавно был предложен экономически эффективный процесс получения катионитов из целлюлозосодержащих материалов, в том числе из древесины, обработкой сырья серной кислотой [9],[10]. В результате такой обработки происходит частичная карбонизация (обугливание) исходного материала и введение в продукт сульфоновокислых групп. Полученные сульфокатиониты, при обработке сырья высококонцентрированной серной кислотой(75-90)% (масс.доли). по своим свойствам не уступают промышленным выпускаемым катионитам[9].
Недостатком предложенного способа является слишком высокая концентрация серной кислоты, по причине которой сильно поднимается стоимость производства, в связи с необходимостью специального оборудования для работы с высококонцентрированными кислотами. Также к недостаткам можно отнести относительно высокий расход серной кислоты (2,7 т на 1 т продукта), удаление которой из продукта требует большого расхода воды (на стадии промывки),вследствие этого могут возникнуть проблемы последующей утилизации значительных объемов сернокислотных растворов.
По этой причине важны исследования по уменьшению расхода кислотного реагента или подбора более оптимального модификатора.
Сокращение расхода кислоты может быть достигнуто использованием в процессе получения катионитов более разбавленных ее растворов. Были проведены исследования и доказано, что обработка исходных материалов водными растворами кислот с концентрацией (20-40)%(масс.доли) позволяет сократить расход кислоты более чем в два раза и получить катионообменники с достаточно высокой обменной емкостью[11],[12]. Применение разбавленных растворов кислоты, на ряду со снижением ее расхода, открывает возможности использования непрореагирующего реагента после отмывки его от продукта водой.
Изучение ионообменных свойств полученных сорбентов показало, что они содержат как сильнокислотные, так и слабокислотные функциональные группы, т.е. являются полифункциональными катионитами[13]. При этом начальная концентрация кислоты в диапазоне от 20 до 90 %(масс.доли) не оказывает существенного влияния на содержание ионогенных групп. В большей степени ионообменная емкость зависит от температуры.
1.3. Сульфокатиониты. Получение и свойства
Сульфокатиониты являются наиболее распространенными сорбентами среди ионитов. Сульфированием достигается введение значительно количества сульфогрупп. Широко применяются полимерные соединения, содержащие сульфогруппы и обладающие свойствами сильных кислот (КУ-1, КУ-2, ДАУЭКС-50, СДВ-3 и др.).
Сульфогруппа (-SО3Н) легче всего вводиться в ароматические углеводороды и их производные, поэтому для синтеза сульфокатионита в качестве сырья используется доступное ароматическое сырье: фенол, стирол, нафталин, антрацен, аценафтен и т.д.
Сульфокатиониты представляет собой твердое вещество, порошок, гранулы, кристаллы или пластины черного цвета, не растворимые в воде. Сульфокатиониты как и все органические иониты обладает рядом свойств характерных именно для этого класса ионообменных материалов.
Одна из важнейших особенностей – максимальная определенность понятия фиксированный ион, поскольку носителем заряда является единичная функциональная группа известного состава и строения.
Вторая особенность – практически полная нерастворимость органических ионитов. Именно для этого класса ионитов представление о фиксированном ионе как о частице не способной пересечь границу раздела ионит – раствор, выполняется с большей точностью.
Вместе с тем каркас органических ионитов, обладает значительной гибкостью и при контакте с таким полярным растворителем как вода, способен к значительному увеличению объема, т. е. набуханию.
В промышленности катиониты получают поликонденсацией соединений с ионогенными группами, полимеризацией виниловых мономеров с ионогенными группами, полимераналогичными превращениями сополимеров винилароматических, винил- и амиллалифатических соединений с дивиниловыми мономерами.
Сульфокислоты бензола и его гомологов для получения сульфокатионитов применяются сравнительно редко, поскольку реакционная способность их невелика, а продукты поликонденсации обладают низкой механической прочностью. Иногда рекомендуют проводить поликонденсацию ароматических углеводородов, а затем сульфировать готовый продукт.
При получении смолы КУ-1 сульфогруппа вводиться в фенол. Затем полученный п-сульфофенол конденсируется с формальдегидом. Таким образом, КУ-1 является катионитом поликонденсационного типа. КУ-1 применяется для очистки воды, сахарных соков, при разрушении алкалоидов.
Сульфокатиониты поликонденсационного типа обладают наибольшей радиационной стойкость. Это, вероятно, объясняется тем, что их сульфогруппы входят в состав исходного соединения. При облучении дозами до 5 — Ю8 рад их полная обменная емкость изменяется незначительно.
Катиониты КУ-2, СДВ, ДАУЭКС-50 получают в виде сферических гранул с различным содержанием звеньев дивинилбензола в сополимере.
Наиболее распространенными среди сорбентов на основе ароматических углеводородов пользуются нафталинформальдегидные иониты. К таким ионитам относятся ионообменные сорбенты марок КУ-5М, КУ-5М, КУ-20, из которых первые два являются продуктами взаимодействия сульфокислот нафталина с формальдегидом в присутствии серной кислоты. Их получают по методу блочной и суспензионной поликонденсации. Ионит КУ-20 синтезирован на основе сульфокислот нафталина и фенола .
В некоторых случаях при получении катионитов применяется инициатор перекись бензоила. Для облегчения сульфирования иногда процесс ведут в растворителе, например, дихлорэтане, который вызывает набухание гранул и облегчает проникновение сульфирующего агента. Также было установлено, что сульфирование раствором S0з в дихлорэтане неочищенных масляных фракций нефти является более мягким по сравнению с сульфированием в газообразном S03, а в полученных сульфонатах несколько увеличивается доля низкомолекулярных кислот.
Сульфокатиониты, представляющие собой продукт сополимеризациисульфофенилметакриламида и длинноцепного сшивающего агента — гексаметилиендиметакриламида, характеризуются как высокой избирательностью сорбции органических ионов, так и высокими скоростями ионообменного процесса, протекающего с их участием.
Представляют определенный практический интерессульфокатиониты, полученные путем конденсации п-фенолсульфокислоты и фурфурола, являющегося доступным и дешевым сырьем.
Значительным прогрессом в отношении создания катионообменных сорбентов органического происхождения явилось предложение использовать продукты сульфирования бурого или спекающегося каменных углей. Сульфирование углей обогащает их структуру дополнительной кислотной группой –SO3H. Процессу сульфирования подвергаются угли, измельченные до частиц диаметром 0,3-1,5 мм. Реакцию проводят в течении 3-4 ч при 150-160оС с четырехкратным (по весу) количеством олеума с 20%-ой концентрацией.
Простота технологического процесса приготовления сульфоуглей, доступность и низкая стоимость исходного сырья, наличие в нем сильнокислотных групп, обеспечивающих полное удаление катионов из раствора, явилось причиной все возрастающего применения сульфоугля в процессах водоумягчения и деминерализации воды.
Так же высокая степень диссоциации водорода сульфогруппы, в отличие от водорода фенольных или карбоксильных групп, дает возмжность проводить катионообменные процессы в сильнокислых средах (до рН=2) и значительно повышает обменную способность фильтров, величина которых возрастает по мере увеличения числа сульфогрупп, введенных в угли.
Таким образом исходя из свойств сульфоугля, он применяется для водоподготовки – умягчения, снижения щелочности и обессоливания воды, применяемой для подпитки котлов на энергетических объектах (ТЭС, ГРЭС, промышленно – отопительные котельные), а также исходной воды для технологических процессов различных отраслей промышленности, в которых требованиями или технологическими регламентами не устанавливается необходимость использования питьевой воды. Также сульфоуголь используется для извлечения ионов тяжелых металлов, в первую очередь меди, цинка, в целлюлозно – бумажной и текстильной промышленности, для очистки сточных вод органических производств и гальванических установок.
Сульфоуголь может применяться в качестве кислотного катализатора различных процессов органического синтеза. Исследование показало каталитическое влияние на самые разнообразные органические реакции. Хотя катиониты обходятся дороже (в расчете на эквивалент водородных ионов), чем серная, соляная или разные сульфокислоты, используемые обычно в качестве катализаторов органических реакций, применение сульфоугля оправдывается во многих случаях благодаря особым преимуществам, вытекающим из его физических и химических свойств. Это доказано практикой нескольких промышленных установок, причем по крайней мере в одной из них катионит работал в качестве катализатора реакции этерификации в течение 5 лет.
Одним из самых большим преимуществ катионитов, в частности сульфоугля является легкость отделения продуктов реакции от катализатора. При периодической работе (партиями) катализатор может быть просто удален простым фильтрованием, причем не требуется никакой дополнительной химической обработки реакционной смеси. Тем самым целиком устраняются трудности, которые обычно встречаются при известковании или других способах нейтрализации растворимых кислот в органической среде. Это преимущество катионитов становится особенно наглядным, когда продукты реакции являются вязкими или высококипящими жидкостями.
Сульфоугли являются хорошими катализаторами реакции этерификации. В числе эфиров полученных в присутствии катализаторов — сульфоуглей, можно назвать триацетин, гликольдиацетат, этилхлорацетат, диметилацетат, бутиловые эфиры высших жирных кислот.
На одной из промышленных установок, где в качестве катализатора при получении нормальных и изобутиловых эфиров жирных кислот применяется «мелочь» сульфоугля, каждая партия катализатора используется около 10 раз, причем необходимость, заменяя, вызывается только механическим измельчением. Поэтому расход катализатора в данном производстве может быть снижен применением катализатора более крупного зернения или переходом к непрерывному процессу[33].
Таким образом, можно сделать вывод, что сульфоуголь можно успешно применять в качестве катализатора для многих реакций, обычно проводимых в присутствии сильных растворимых кислот. Он обладает рядом ценных физических и химических свойств, и поэтому ему во многих случаях отдают предпочтение, не смотря на то, что он дороже в расчете на эквивалент водорода, чем обычные кислоты – катализаторы.
1.4. Альтернативные способы получения сульфокатионитов
Альтернативный метод предложен в диссертационной работе Крайновой Е. А. «Разработка технологии сульфокатионитов методом сернокислого обугливания различных видов целлюлозосодержащих твёрдых отходов». Работа была выполнена в Российском химико-технологическом университете им. Д. И. Менделеева
Известно, что сульфоугли можно получать из целлюлозосодержащих материалов, в том числе из отходов производства и потребления, с использованием серной кислоты вместо олеума.
Основные стадии получения сульфокатионита: разложение и сульфирование; промывка; сушка. Проведенные структурные исследования показали, что полученный углеродосодержащий материал состоит из углеродных микрокристаллов с размером частиц от 0,5 до 2 мм и имеет размер пор от 1 до 1000 нм. Степень разложения сырья зависит от температуры процесса и времени контакта фаз, удельного массового расхода и начальной концентрации серной кислоты.
В данной работе показано, что изменение начальной концентрации серной кислоты от 75% (масс.доли) до 95% (масс.доли) существенно не влияет на степень полезно используемого сырья. При этом целесообразно проводить реакцию при температуре (85±5) оС, времени контакта фаз 30 минут, использовать удельный массовый расход серной кислоте в пределах (3,05±0,25)кг(H2SO4)∙кг(БС)-1 в пересчете на моногидрат серной кислоты.
Показано, что при значении начальной концентрации серной кислоты равной (70±5)% (масс.доли), статическая обменная емкость (СОЕ) составляет 6,0 мг-экв∙г-1.
Предложен гипотетический механизм процесса получения сульфокатионита, согласно которому на стадии разложения (дегидратации) и сульфирования образуется гетерогенная смесь (полуфабрикат), содержащая сульфокатионит и отработанную серную кислоту (ОСК).
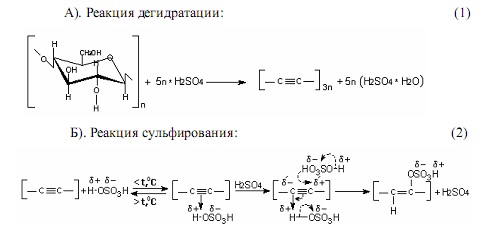
Определено, что промывка водой полуфабриката должна обеспечивать не только удаление отработанной серной кислоты, но и растворимых в нейтральных и щелочных растворах полупродуктов разложения. Предложена двухстадийная замкнутая схема промывки полуфабрикатов. На первой стадии с холодной водой удаляется отработанная серная кислота, на второй стадии с водой, нагретой до (85±5) °С, вымываются органические примеси. Такая промывка обеспечивает использование сульфокатионита в кислых и слабощелочных средах.
Сушку сульфокатионита от влажности (65±5) %(масс.доли) до (35±5) % (масс.доли)можно проводить в течение 15 часов в естественных условиях или в сушилке при температуре (110±5) °С в течение одного часа.
Разработана технологическая схема производства сульфокатионита в Н+-форме.
Установка по производству углеродного сульфокатионита рассчитана на переработку в непрерывном режиме 205,5 кг∙ч-1 сырья при его обугливании 800,0 кг∙ч-1 75% (масс.доли) серной кислотой при температуре (85±5) °С и времени контакта фаз 30 мин после смешения реагентов.
Поверхность аппаратов футеруют кислоупорной эмалью и образующейся самопроизвольно накипью из сульфата кальция.
По такой схеме получается 234,6 кг∙ч-1сульфокатионита с остаточной влажностью (35±5)%(масс.доли).
Основные расходные коэффициенты на тонну сульфокатионита: ЦТО – 1,4 т (влажностью около 10%(масс.доли)); серной кислоты (75% (масс.доли)) – 3,6 т; свежей воды для подпитки 37,13 м3; электроэнергии – 1,6 МВт∙ч. На тонну сульфокатионита образуется продувочной воды – 16,71 м3.
Рассчитана себестоимость сульфокатионита, которая в 1,7 раз ниже себестоимости выпускаемых в промышленности сульфоуглей обработкой каменных углей 20%-ым олеумом.
1.5. Фосфорнокислые катиониты
Как уже упоминалось выше, существует проблема производства сульфокатионитов в связи с определенными сложностями, вызванными работой с серной кислоты. Возвращаясь к различным методам решения этой проблемы, есть возможность выбора другого модификатора, более оптимального с экономической точки зрения, для исходного материала.
В качестве модификаторов используются различные соединения, такие как: серная кислота, фосфорная кислота, хлористый цинк и др. Наиболее качественным модификатором является фосфорная кислота. Процесс модификации обычно сопровождается химическими изменениями компонентов древесины. Под влиянием химических изменений меняются также физико-механические и технологические свойства. Модификация способствует устранению первичной структуры сырья (уменьшение количества макропор), снижает образование дегтя и других смолистых веществ[15].
Фосфорнокислые катиониты занимают особое место среди известных в настоящее время ионитов. Они обладают всеми свойствами сильно- и слабокислотных катионитов. Для них характерны высокая обменная емкость, селективность к ряду металлов. Фосфорнокислые катиониты обладают комплексообразующими свойствами. Вследствие повышенной селективности ко многим ионам тяжелых и переходных металлов представляется перспективным их применение в различных отраслях народного хозяйства и научных исследованиях [14].
Фосфорнокислые катиониты превосходят сульфо- и карбоксильные катиониты по стойкости к сильным электролитам и окислителям.
Синтез фосфорсодержащих катионитов может быть осуществлен следующими способами: полимераналогичными превращениями полимеров, не содержащих функциональных групп, полимеризацией фосфорсодержащих мономеров и поликонденсацией фосфорсодержащих исходных соединений.
Наибольшее распространение получил первый способ, который широко применяется для производства промышленных марок фосфорнокислотных катионитов. Фосфорнокислотные катиониты получаются обработкой трехмерных сополимеров стирола с девинилбензолом или продуктов их хлорметилирования треххлористым фосфором с последующим омылением в присутствии окислителей.
Перспективными являются методы синтеза фосфорнокислых ионитов путем химических превращений поливинилфенилдихлорфосфина, полученного в качестве промежуточного продукта при синтезе катионита с поливинилфенилфосфоновыми группами.
В данной дипломной работе фосфорнокислые катиониты получены методом модификации смеси гидролизного лигнина с хвоей и дальнейшей термообработкой.
или напишите нам прямо сейчас:
⚠️ Пожалуйста, пишите в MAX или заполните форму выше.
В России Telegram и WhatsApp блокируют - сообщения могут не дойти.
